
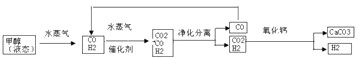
£Ø13·Ö£© ¹¤ŅµŌĮĻ¼×“¼æÉŅŌÓėĖ®ÕōĘų·“Ӧɜ³ÉĒāĘų£¬·“Ó¦·½³ĢŹ½ČēĻĀ£ŗ
CH3OH(g)£«H2O(g) ![]() CO2(g)£«3H2(g) ”÷H > 0
CO2(g)£«3H2(g) ”÷H > 0
£Ø1£©Ņ»¶ØĢõ¼žĻĀ£¬ĻņĢå»żĪŖ2 LµÄŗćČŻĆܱÕČŻĘ÷ÖŠ³äČė1 mol CH3OH(g)ŗĶ3 mol H2O(g)£¬20 sŗ󣬲āµĆ»ģŗĻĘųĢåµÄŃ¹ĒæŹĒ·“Ó¦Ē°µÄ1.2±¶£¬ŌņÓĆ¼×“¼±ķŹ¾µÄ·“Ó¦ĖŁĀŹ ”£
£Ø2£©ÓŅĶ¼ÖŠPŹĒæÉ×ŌÓÉĘ½ŠŠ»¬¶ÆµÄ»īČū£¬¹Ų±ÕK£¬ŌŚĻąĶ¬ĪĀ¶ČĻĀ£¬ĻņAČŻĘ÷ÖŠ³äČė1 mol CH3OHŗĶ2 mol H2O(g)£¬ĻņBČŻĘ÷ÖŠ³äČė1.2 mol CH3OH(g)ŗĶ2.4 mol H2O(g)£¬Į½ČŻĘ÷·Ö±š·¢ÉśÉĻŹö·“Ó¦”£ŅŃÖŖ£¬ĘšŹ¼Ź±ČŻĘ÷AŗĶBµÄĢå»ż¾łĪŖa L”£ŹŌ»Ų“š£ŗ

¢Ł ·“Ó¦“ļµ½Ę½ŗāŹ±£¬ČŻĘ÷BµÄĢå»żĪŖ1.5 a L£¬BČŻĘ÷ÖŠCH3OH×Ŗ»ÆĀŹĪŖ £¬A”¢BĮ½ČŻĘ÷ÖŠH2O(g)µÄĢå»ż°Ł·Öŗ¬ĮæµÄ“󊔹ŲĻµĪŖB A£ØĢī”°£¾”±”¢”°£¼”±”¢”°£½”± £©
¢Ś Čō“ņæŖK£¬Ņ»¶ĪŹ±¼äŗóÖŲŠĀ“ļµ½Ę½ŗā£¬ČŻĘ÷BµÄĢå»żĪŖ L£ØĮ¬ĶعÜÖŠĘųĢåĢå»żŗöĀŌ²»¼Ę£¬ĒŅ²»æ¼ĀĒĪĀ¶ČµÄÓ°Ļģ£©”£
£Ø3£©ĻĀĆęĖÄøöŃ”ĻīŹĒĖÄĪ»Ń§ÉśŌŚŃ§Ļ°»Æѧ·“Ó¦ĖŁĀŹÓė»Æѧ·“Ó¦ĻŽ¶ČŅŌŗó£¬ĮŖĻµ»Æ¹¤Éś²śŹµ¼ŹĖł·¢±ķµÄæ“·Ø£¬ÄćČĻĪŖ²»ÕżČ·µÄŹĒ_______
A.»Æѧ·“Ó¦ĖŁĀŹĄķĀŪæÉÖøµ¼ŌõŃłŌŚŅ»¶ØŹ±¼äÄŚæģ³ö²śĘ·
B.ÓŠŠ§ÅöײĄķĀŪæÉÖøµ¼ŌõŃłĢįøßŌĮĻµÄ×Ŗ»ÆĀŹ
C.ĄÕĻÄĢŲĮŠŌĄķæÉÖøµ¼ŌõŃłŹ¹ÓĆÓŠĻŽŌĮĻ¶ą³ö²śĘ·
D.ÕżČ·ĄūÓĆ»Æѧ·“Ó¦ĖŁĀŹŗĶ»Æѧ·“Ó¦ĻŽ¶Č¶¼æÉŅŌĢįø߻ƹ¤Éś²śµÄ×ŪŗĻ¾¼ĆŠ§Ņę
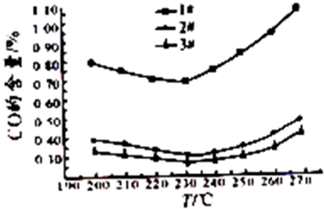
£Ø4)¼×“¼µČÓŠ»śĪļŌŚæÕĘųÖŠČ¼ÉÕŹ±ÓÉÓŚČ¼ÉÕ²»³ä·ÖæÉÄÜ»į²śÉśCOµČĪŪČ¾Īļ”£ÓŠČĖĢį³ö£¬æÉŅŌÉč¼Ę·“Ó¦2CO£½2C£«O2£Ø”÷H£¾0”¢”÷S£¼0£©Ą“Ļū³żCOµÄĪŪČ¾”£ĒėÄćÅŠ¶ĻŹĒ·ńæÉŠŠ²¢Ėµ³öĄķÓÉ£ŗ________________”£
 ŠĀæĪ±źĶ¬²½ŃµĮ·ĻµĮŠ“š°ø
ŠĀæĪ±źĶ¬²½ŃµĮ·ĻµĮŠ“š°ø Ņ»ĻßĆūŹ¦æŚĖćÓ¦ÓĆĢāĢģĢģĮ·Ņ»±¾Č«ĻµĮŠ“š°ø
Ņ»ĻßĆūŹ¦æŚĖćÓ¦ÓĆĢāĢģĢģĮ·Ņ»±¾Č«ĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
| ±½¼×Ėį | ¼×“¼ | ±½¼×Ėį¼×õ„ | |
| ČŪµć/”ę | 122.4 | -97 | -12.3 |
| ·Šµć/”ę | 249 | 64.3 | 199.6 |
| ĆܶČ/g£®cm-3 | 1.2659 | 0.792 | 1.0888 |
| Ė®ČÜŠŌ | Ī¢ČÜ | »„ČÜ | ²»ČÜ |



²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
| Ź±¼ä s | 0 | 1 | 2 | 3 | 4 | 5 |
| C£ØCH3OH£© /mol£®L-1 |
1.00”Į10-3 | 4.50”Į10-4 | 2.5 0”Į10-4 | 1.50”Į10-4 | 1.00”Į10-4 | 1.00”Į10-4 |
| C£ØH2O£© mol£®L-1 | 3.60”Į10-3 | 3.05”Į10-3 | 2.85”Į10-3 | 2.75”Į10-3 | 2.7”Į10-3 | 2.7”Į10-3 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ½ĖÕŹ”Ēå½ÖŠŃ§2008£2009ѧğµŚ¶žŃ§ĘŚø߶ž»ÆѧµŚ2“ĪŌĀæ¼ŹŌ¾ķ ĢāŠĶ£ŗ022
¹¤ŅµŌĮĻ¼×“¼æÉŅŌÓėĖ®ÕōĘų·“Ӧɜ³ÉĒāĘų£¬·“Ó¦·½³ĢŹ½ČēĻĀ£ŗ
CH3OH(g)£«H2O(g)![]() CO2(g)£«3H2(g)””¦¤H£¾0
CO2(g)£«3H2(g)””¦¤H£¾0
(1)Ņ»¶ØĢõ¼žĻĀ£¬ĻņĢå»żĪŖ2 LµÄŗćČŻĆܱÕČŻĘ÷ÖŠ³äČė1 mol””CH3OH(g)ŗĶ3 mol””H2O(g)£¬20 sŗ󣬲āµĆ»ģŗĻĘųĢåµÄŃ¹ĒæŹĒ·“Ó¦Ē°µÄ1.2±¶£¬ŌņÓĆ¼×“¼±ķŹ¾µÄ·“Ó¦ĖŁĀŹĪŖ________£»
(2)ÅŠ¶Ļ(1)ÖŠæÉÄę·“Ó¦“ļµ½Ę½ŗāדĢ¬µÄŅĄ¾ŻŹĒ________(ĢīŠņŗÅ)£»
¢ŁvÕż(CH3OH)£½vÕż(CO2)
¢Ś»ģŗĻĘųĢåµÄĆÜ¶Č²»±ä
¢Ū»ģŗĻĘųĢåµÄĘ½¾łĻą¶Ō·Ö×ÓÖŹĮæ²»±ä
¢ÜCH3OH”¢H2O”¢CO2”¢H2µÄÅØ¶Č¶¼²»ŌŁ·¢Éś±ä»Æ
(3)Ķ¼ÖŠPŹĒæÉ×ŌÓÉĘ½ŠŠ»¬¶ÆµÄ»īČū£¬¹Ų±ÕK£¬ŌŚĻąĶ¬ĪĀ¶ČĻĀ£¬ĻņAČŻĘ÷ÖŠ³äČė1 mol””CH3OHŗĶ2 mol””H2O(g)£¬ĻņBČŻĘ÷ÖŠ³äČė1.2 mol””CH3OH(g)ŗĶ2.4 mol””H2O(g)£¬Į½ČŻĘ÷·Ö±š·¢ÉśÉĻŹö·“Ó¦£®ŅŃÖŖ£¬ĘšŹ¼Ź±ČŻĘ÷AŗĶBµÄĢå»ż¾łĪŖa L£®ŹŌ»Ų“š£ŗ

¢Ł·“Ó¦“ļµ½Ę½ŗāŹ±£¬ČŻĘ÷BµÄĢå»żĪŖ1.5a L£¬BČŻĘ÷ÖŠCH3OH×Ŗ»ÆĀŹĪŖ________£¬A”¢BĮ½ČŻĘ÷ÖŠH2O(g)µÄĢå»ż°Ł·Öŗ¬ĮæµÄ“󊔹ŲĻµĪŖB________A(Ģī”°£¾”±”¢”°£¼”±”¢”°£½”±)£»
¢ŚČō“ņæŖK£¬Ņ»¶ĪŹ±¼äŗóÖŲŠĀ“ļµ½Ę½ŗā£¬ČŻĘ÷BµÄĢå»żĪŖ________L(Į¬ĶعÜÖŠĘųĢåĢå»żŗöĀŌ²»¼Ę£¬ĒŅ²»æ¼ĀĒĪĀ¶ČµÄÓ°Ļģ)£®
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com