
【题目】下列各组离子一定能大量共存的是( )
A.在无色溶液中:NH4+、Fe2+、SO42﹣、CO32﹣
B.在含大量Ba2+的溶液中:NH4+、Na+、Cl﹣、NO3﹣
C.在强碱溶液中:Na+、K+、Cl﹣、HCO3﹣
D.在pH=1的溶液中:K+、Fe2+、Cl﹣、CH3COO﹣
 期末100分闯关海淀考王系列答案
期末100分闯关海淀考王系列答案 小学能力测试卷系列答案
小学能力测试卷系列答案科目:高中化学 来源: 题型:
【题目】元素X的原子有3个电子层,最外层有4个电子.这种元素位于周期表的( )
A.第4周期ⅢA族
B.第4周期ⅦA族
C.第3周期Ⅳ族
D.第3周期ⅣA族
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】据报道,某国一集团拟在太空建造巨大的激光装置,把太阳光变成激光用于分解海水制氢:2H2O![]() 2H2↑+O2↑,下列说法正确的是( )
2H2↑+O2↑,下列说法正确的是( )
①水的分解反应是放热反应
②氢气是一级能源
③使用氢气作燃料有助于控制温室效应
④若用生成的氢气与空气中多余的二氧化碳反应生成甲醇储存起来,可以改善生存环境
A. ①② B. ②③ C. ①③ D. ③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学兴趣小组设计实验,测定Na2CO3与NaHCO3混合物中Na2CO3的质量分数。
甲方案:
实验步骤为:①称量空坩埚的质量为A g
②称量装有试样的坩埚质量为B g ③加热
④冷却⑤称量坩埚和残余物的质量为C g
⑥重复③至⑤操作,直至恒重,质量为D g
(1)坩埚中发生反应的化学方程式为__________________。
(2)计算Na2CO3质量分数必须用到的测定数据为___________(填“A”、“B”、“C”或“D”)。
乙方案:
在天平上准确称取0.3000 g样品,放入锥形瓶中,加入适量水溶解,滴入2滴酚酞试液,用0.1000 mo1·L-1,的标准盐酸滴定至溶液由粉红色刚好变为无色,达到滴定终点时产物为NaHCO3。重复上述操作两次,消耗盐酸的体积为20.00 mL。
(3)配制上述盐酸标准溶液100 mL,若用2.0 mol·L-1HCl进行配制,需用滴定管量取该HCl溶液________mL;定容时俯视刻度线,将导致配制的溶液浓度___________(填“偏高”、“偏低”或“没有影响”)。
(4)样品中Na2CO3的质量分数为___________(用百分数表示,精确到0.1%)。
丙方案:
称取m g样品,选用下图部分装置测定样品与硫酸反应生成的气体体积。
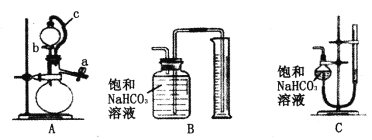
(5)某同学按以下方法检查装置A的气密性:在分液漏斗中加入适量水,如图连接好装置,关闭止水夹a,用止水夹夹住橡皮管c,打开活塞b。若装置不漏气,则观察到的现象为__________________。实验时,装置A中c的作用_____________、_____________。
(6)为了提高测定的准确性,应选用装置A和__________(填写字母标号)进行实验。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】若NA表示阿伏加德罗常数,下列叙述正确的是( )
A.1 mol NH3与1 mol OH-所含的质子数均为10NA
B.标准状况下,22.4L CHCl3中含C—H键数目为NA
C.1mol Fe与足量的稀HNO3反应时,转移3NA个电子
D.常温下,pH=13的NaOH溶液中含OH-数目为0.1NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在常温下,发生下列几种反应
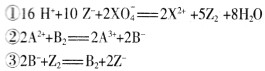
根据上述反应,下列结论判断错误的是
A.溶液中可发生:Z2+2A2+=2A3++2Z-
B.Z2在①③反应中为氧化剂
C.氧化性强弱的顺序为:XO4->Z2>B2>A3+
D.X2+是XO4-的还原产物
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com