
【题目】将一份CaCO3粉末放入500mL的盐酸中,恰好完全反应,在标准状况下收集到的CO2 气体体积为22.4L,求
(1)CaCO3的质量.
(2)盐酸物质的量浓度.
【答案】
(1)解:设生成22.4LCO2气体需要碳酸钙的质量为mg,则:
CaCO3 | + | 2HCl | = | CaCl2 | + | H2O | + | CO2↑ |
100g | 22.4L | |||||||
mg | 22.4L |
所以100g:mg=22.4L:22.4L
解得:x=100
答:需要碳酸钙的质量为100g
(2)解:设生成22.4LCO2气体需要HCl的物质的量为nmol,则:
CaCO3 | + | 2HCl | = | CaCl2 | + | H2O | + | CO2↑ |
2mol | 22.4L | |||||||
nmol | 22.4L |
所以2mol:nmol=22.4L:22.4L
解得:n=2
所以该盐酸的物质的量浓度为: ![]() =4mol/L,
=4mol/L,
答:该盐酸的物质的量浓度为4mol/L
【解析】(1)令碳酸钙的质量为mg,根据反应CaCO3+2HCl=CaCl2+H2O+CO2↑计算;(2)根据反应CaCO3+2HCl=CaCl2+H2O+CO2↑计算HCl的物质的量,再根据c= ![]() 计算盐酸的浓度.
计算盐酸的浓度.


科目:高中化学 来源: 题型:
【题目】若NA表示阿伏伽德罗常数的值,下列说法正确的是( )
A.常温下,0.1mol Fe与酸完全反应时,失去的电子数一定为0.3NA
B.0.1mol/L的 CaCl2溶液中所含Cl﹣数为0.2NA
C.7.8g Na2O2与足量水反应,转移电子数为0.2NA
D.常温常压下,8g CH4含有的分子数为0.5NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CH4、H2、C都是优质的能源物质,它们燃烧的热化学方程式为:
①2CH4(g)+4O2(g)═2CO2(g)+4H2O(l)△H=﹣890.3kJmol﹣1
②2H2(g)+O2(g)═2H2O(l)△H=﹣571.6kJmol﹣1
③C(s)+O2(g)═CO2(g)△H=﹣393.5Kjmol﹣1
(1)在深海中存在一种甲烷细菌,它们依靠酶使甲烷气体与O2作用而产生的能量存活,甲烷细菌使1mol甲烷生成CO2气体与液态水,放出的能量(填“>”、“<”或“=”)890.3kJ.
(2)甲烷与CO2可用于合成合成气(主要成分是一氧化碳和氢气):CH4+CO2═2CO+2H2 , 1g CH4完全反应可释放15.46kJ的热量,则:
①图1(所有物质均为气态)能表示该反应过程中能量变化的是(填字母).
②若将物质的量均为1mol的CH4与CO2充入某恒容密闭容器中,体系放出的热量随时间的变化如图2所示,则CH4的转化率为 .
(3)C(s)与H2(g)不反应,所以C(s)+2H2(g)═CH4(g)的反应热无法直接测量,但通过上述反应可求出C(s)+2H2(g)═CH4(g)的反应热△H= .
(4)目前对于上述三种物质的研究是燃料研究的重点,下列关于上述三种物质的研究方向中可行的是(填字母).
A.寻找优质催化剂,使CO2与H2O反应生成CH4与O2 , 并放出热量
B.将固态碳合成为C60 , 以C60作为燃料
C.寻找优质催化剂,利用太阳能使大气中的CO2与海底开采的CH4合成合成气(CO、H2)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】补充完成下表:
元素 | 甲 | 乙 | 丙 |
元素符号 | ① | ② | O |
原子结构 |
| ③ | ④ |
周期 | 三 | 三 | ⑤ |
族 | ⑥ | ⅦA | ⑦ |
(1)请把序号①一⑦的答案对应填上) ①②③④⑤⑥⑦
(2)甲元素最高价氧化物对应的水化物呈性(填“酸、碱”),乙元素的最高价氧化物对应的水化物的化学式为 .
(3)甲与乙两元素的单质反应生成物的电子式为 , 属于(离子或共价)化合物.
(4)甲单质与丙的氢化物反应的化学方程式为
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物A~E间的转化关系如下图所示。A是石油裂解气的主要成分,其产量通常用来衡量一个国家的石油化工水平。E为生活中常用的有机高分子化合物。
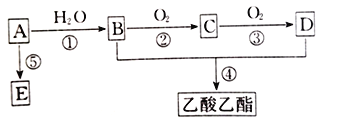
回答下列问题:
(1)A的名称是__________;将A通入溴的四氯化碳溶液中,现象为________。
(2)写出E的结构简式:__________________________。
(3)④的反应类型为______________,写出其化学方程式________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为维持人体血液中的血糖含量,在给病人输液时,通常用葡萄糖注射液.如图是医院病人输液使用的一瓶质量分数为6%的葡萄糖(C6H12O6相对分子质量为180)注射液标签,请认真观察标签上所列内容后计算:
(1)该溶液的物质的量浓度为molL﹣1 .
(2)该溶液的密度为gmL﹣1(精确到0.1g).
(3)如果从该瓶中取出75g葡萄糖注射液,将其变为15%的注射液,需要加入g葡萄糖固体(精确到0.1g).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2017年世界环境日主题是“人与自然,相联相生” 。下列做法应该提倡的是( )
A. 将工业废液直接排入海洋以减少河道污染 B. 推广使用高效、低毒农药,减轻水体污染
C. 将废旧电池集中深埋,可防止重金属污染 D. 增高燃煤锅炉烟囱,将废气直接排到高空
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】试根据以下信息进行判断:下列为A、B、C、D四种物质的转化关系,a、b为反应条件,
(1)若A为气态化合物,B到C转化不需要条件,则A为(填写化学式),写出工业合成A化学方程式 , 写出Cu+D溶液→B的离子方程式
(2)把某黑色固体Y加热至红热,投入到上述某种黄色溶液D中产生两种气体组成的混合气体X,将X作如下所示实验:
写出下列物质的化学式YN;写出黑色固体Y与黄色溶液D反应的化学方程式 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定条件下,PbO2与Cr3+反应,产物是Cr2O72-和Pb2+,则与1moLCr3+反应所需PbO2的物质的量为
A. 3.0moL B. 1.5moL C. 1.0moL D. 0.75moL
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com