
| X | ||
| Y | Z | W |
| A. | X、Z、W的简单氢化物的稳定性Z>W>X | |
| B. | X元素的单质在化学反应中只表现还原性 | |
| C. | X、Y的简单离子半径Y>X | |
| D. | Y、Z、X的最高价氧化物均能与NaOH溶液反应 |
分析 X、Y、Z、W四种短周期元素中,Z的单质是常见的半导体材料,则Z为Si,由元素在元素周期表中的相对位置,可知X为N元素、Y为Al、W为P元素.
A.非金属性越强,氢化物越稳定;
B.氮气中N元素化合价为0,反应中化合价可以升高,也可以降低;
C.电子层结构相同,核电荷数越大离子半径越小,电子层越多离子半径越大;
D.Y、Z、X的最高价氧化物分别为氧化铝、二氧化硅、五氧化二氮,均能与NaOH溶液反应.
解答 解:X、Y、Z、W四种短周期元素中,Z的单质是常见的半导体材料,则Z为Si,由元素在元素周期表中的相对位置,可知X为N元素、Y为Al、W为P元素.
A.同周期自左而右非金属性增强,同主族自上而下非金属性减弱,故非金属性Z<W<X,非金属性越强,氢化物越稳定,简单氢化物的稳定性Z<W<X,故A错误;
B.氮气中N元素化合价为0,反应中化合价可以升高,也可以降低,如与氧气反应生成NO,表现还原性,与氢气生成氨气,表现氧化性,故B错误;
C.N3-、Al3+电子层结构相同,核电荷数越大离子半径越小,故离子半径:N3->Al3+,故C错误;
D.Y、Z、X的最高价氧化物分别为氧化铝、二氧化硅、五氧化二氮,氧化铝属于两性氧化物,能与NaOH溶液反应,二氧化硅、五氧化二氮属于酸性氧化物,能与氢氧化钠溶液反应,故D正确,
故选D.
点评 本题考查物质结构性质关系,推断元素是解题关键,注意对元素周期律的理解掌握,掌握微粒半径比较规律,难度不大.


科目:高中化学 来源: 题型:解答题
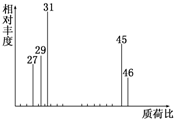 为了测定某有机物A的结构,做如下实验:
为了测定某有机物A的结构,做如下实验:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 117 g该元素原子的物质的量为1 mol | |
| B. | 该元素一定为非金属元素 | |
| C. | 该元素在地球上的含量十分丰富 | |
| D. | 该元素的金属性可能比非金属性更明显 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
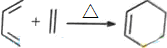 .根据下列转化流程,回答问题:
.根据下列转化流程,回答问题: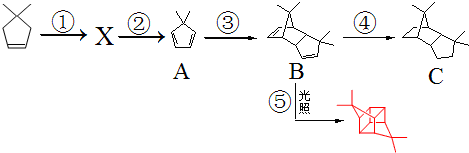
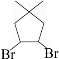 .
.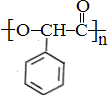 的合成路线:
的合成路线: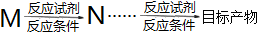 )
)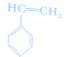 $\stackrel{Br_{2}}{→}$
$\stackrel{Br_{2}}{→}$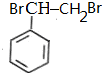 $→_{△}^{NaOH溶液}$
$→_{△}^{NaOH溶液}$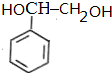 $\stackrel{[O]}{→}$
$\stackrel{[O]}{→}$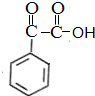 $→_{催化剂}^{H_{2}}$
$→_{催化剂}^{H_{2}}$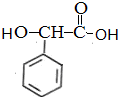 $\stackrel{浓H_{2}SO_{4}△}{→}$
$\stackrel{浓H_{2}SO_{4}△}{→}$ .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
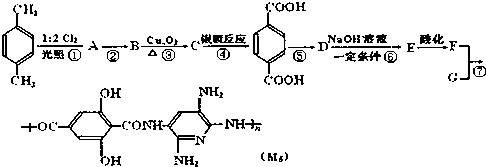
 ,
, ;F的含氧官能团的名称有羧基、(酚)羟基.
;F的含氧官能团的名称有羧基、(酚)羟基. .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 聚丙烯的结构简式: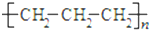 | |
| B. | 乙炔的分子结构模型示意图: | |
| C. | H2O2的电子式:H+[${\;}_{•}^{•}$$\underset{\stackrel{••}{O}}{••}$${\;}_{•}^{•}$$\underset{\stackrel{••}{O}}{••}$${\;}_{•}^{•}$]2-H+ | |
| D. |  的名称:3-甲基-1-丁醇 的名称:3-甲基-1-丁醇 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
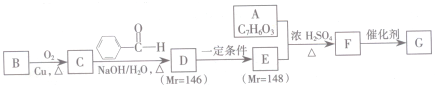

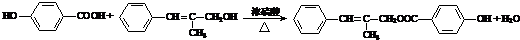 .
. .
. (其中任一种).
(其中任一种).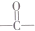 结构②苯环上有2个取代基.
结构②苯环上有2个取代基.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
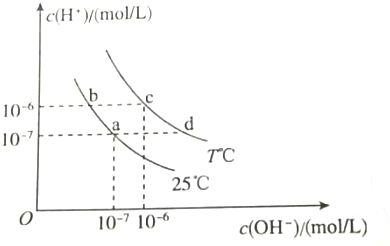
| A. | a点对应的溶液中:Al3+、Na+、Cl-、CO32- | |
| B. | b点对应的溶液中:K+、Ba2+、NO3-、AlO2- | |
| C. | c点对应的溶液中:Fe3+、Na+、I-、SO42- | |
| D. | d点对应的溶液中:Na+、K+、SO32-、Cl- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com