
【题目】一种新型环保电池是采用低毒的铝合金(丢弃的易拉罐)、家庭常用的漂白水、食盐、氢氧化钠(化学药品店常见试剂)等原料制作的。电池的总反应方程式为2Al+3ClO-+2OH-=3Cl-+2AlO2-+H2O。下列说法不正确的是( )
A. 该电池的优点是电极材料和电解质用完后可以更换
B. 该电池发生氧化反应的是金属铝
C. 电极的正极反应式为3ClO-+3H2O+6e-=3Cl-+6OH-
D. 当有0.1 mol Al完全溶解时,流经电解液的电子个数为1.806×1023
 初中暑期衔接系列答案
初中暑期衔接系列答案科目:高中化学 来源: 题型:
【题目】全世界每年被腐蚀损耗的钢铁材料约占全年钢铁产量的十分之一.研究钢铁的腐蚀及防护有重要意义.回答下列问题:
(1)钢铁发生腐蚀的主要类型是电化学腐蚀,在电化学腐蚀中,负极反应是 , 正极反应是 .
(2)某实验小组设计图1实验探究铁生锈的条件: 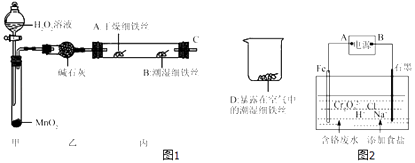
反应4min后观察,发现A处铁丝依然光亮,B处铁丝表面灰暗,D处铁丝依然光亮.该实验说明铁生锈主要与和有关;B、D处实验现象对比说明:决定铁生锈的一个重要因素是 .
(3)金属及塑料制品表面镀铬不仅美观还可提高金属制品抗腐蚀性能.常见镀铬液由重铬酸(H2Cr2O7)和催化剂硫酸组成.
①重铬酸中,Cr元素的化合价为 .
②镀铬时由CrO42﹣放电产生铬镀层.阴极的电极反应式为 .
(4)电镀废水中Cr2O72﹣具有高毒性,必须经处理后才能排放.电解法处理含铬的强酸性废水的原理如图2所示.
电解产生的Fe2+将Cr2O72﹣还原为Cr3+ , 再随着溶液pH的升高,便有Fe(OH)3和Cr(OH)3沉淀生成.
①图中A为电源极;电解时阴极产生的气体为(写化学式).
②写出Fe2+与Cr2O72﹣反应的离子方程式: .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用铜片、银片、Cu(NO3)2溶液、AgNO3溶液、导线和盐桥(装有琼脂﹣KNO3的U形管)构成一个原电池(如图).以下有关该原电池的叙述正确的是
①在外电路中,电子由铜电极流向银电极
②正极反应为:Ag++e﹣=Ag
③实验过程中取出盐桥,原电池仍继续工作
④将铜片浸入AgNO3溶液中发生的化学反应与该原电池反应相同( )
A.①②
B.①②④
C.②③
D.①③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验与对应示意图的关系正确的是( )
A | B | C | D |
NaAlO2溶液中逐滴滴加盐酸至过量 | AlCl3溶液中逐滴滴加氨水至过量 | 明矾溶液中逐滴滴加Ba(OH)2溶液至过量 | 澄清石灰水中缓慢通入CO2至过量 |
|
|
|
|
A.A
B.B
C.C
D.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】海水开发利用的部分过程如图所示.下列说法错误的是( ) 
A.向苦卤中通入Cl2是为了提取溴
B.粗盐可采用除杂和重结晶等过程提纯
C.工业生产常选用NaOH作为沉淀剂
D.富集溴一般先用空气和水蒸气吹出单质溴,再用SO2将其还原吸收
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“探险队员”﹣盐酸,不小心走进了化学迷宫,不知怎样走出来,因为迷宫有许多“吃人的野兽”(即能与盐酸反应的物质或者是水溶液),盐酸必须避开它们,否则就无法通过.
(1)在能“吃掉”盐酸的化学反应中,属于酸碱中和反应的有个,属于氧化还原反应的有个,其中能“吃掉”盐酸的盐是(填化学式),写出该反应的离子方程式 .
(2)在不能与盐酸反应的物质中,属于电解质的是(填写物质序号,下同),属于非电解质的是 .
(3)请你帮助它走出迷宫(用图中物质前的序号连接起来表示所走的路线) .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用铜片、银片、Cu(NO3)2溶液、AgNO3溶液、导线和盐桥(装有琼脂﹣KNO3的U形管)构成一个原电池(如图).以下有关该原电池的叙述正确的是
①在外电路中,电子由铜电极流向银电极
②正极反应为:Ag++e﹣=Ag
③实验过程中取出盐桥,原电池仍继续工作
④将铜片浸入AgNO3溶液中发生的化学反应与该原电池反应相同( )
A.①②
B.①②④
C.②③
D.①③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】己知丙酮(C3H6O)无色液体,可溶于水,密度小于lg/mL,沸点约为56℃,要从水与丙酮的混合物里将丙酮分离出来,下列方法最合理的是
A. 蒸馏 B. 分液 C. 过滤 D. 蒸发
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在恒容密闭容器中通入X并发生反应:2X(g)Y(g),温度T1、T2下X的物质的量浓度c(X)随时间t变化的曲线如图所示.下列叙述正确的是( ) 
A.该反应进行到M点放出的热量大于进行到W点放出的热量
B.T2下,在0~t1时间内,v(Y)= ![]() mol?L﹣1?min﹣1
mol?L﹣1?min﹣1
C.M点的正反应速率V正大于N点的逆反应速率V逆
D.M点时再加入一定量X,平衡后X的转化率减小
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com