
| A、2s22p2和2s22p4 |
| B、3s1和3s23p4 |
| C、3s23p4和2s22p4 |
| D、3s2和2s22p5 |


 阳光课堂课时作业系列答案
阳光课堂课时作业系列答案科目:高中化学 来源: 题型:
| A、c(Na+)=c(CH3COO-) |
| B、原NaOH溶液的浓度为0.5 mol/L |
| C、原溶液中c(CH3COO-)>c(OH-) |
| D、原NaOH溶液的浓度小于0.5 mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 0.01mol?L-1的溶液 | X | Y | Z | W |
| PH | 12 | 2 | 8.5 | 4.5 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、硝酸钠与稀盐酸的混合溶液:c(Na+)+c(H+)=c(NO3-)+c(Cl-)+c(OH-) |
| B、0.1mol/LNaHCO3溶液:c(HCO3-)+c(CO32-)+c(OH-)>c(Na+)+c(H+)+c(H2CO3) |
| C、等体积、等物质的量浓度的NaX 和弱酸HX混合的溶液中:c(Na+)>c(HX)>c(X-)>c(H+)>c(OH-) |
| D、相同条件下pH=5的①NH4Cl溶液②CH3COOH溶液③稀盐酸,三种溶液中由水电离产生的c(H+):①>②>③ |
查看答案和解析>>
科目:高中化学 来源: 题型:
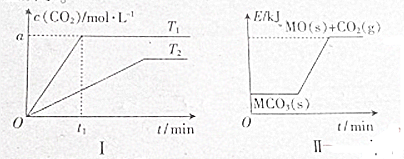
| A、图象Ⅰ中的温度:T1<T2 |
| B、T2时缩小容积’重新达到平衡时c(CO2)增大 |
| C、T1时该反应的平衡常数K=a |
| D、T1和T2温度下平衡常数:K1<K2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 选项 | 条件 | 离子组 | 离子共存判断及反应的离子方程式 |
| A | 滴加氨水 | Na+、Al3+、Cl-、 NO3- | 不能大量共存,Al3++3OH-═Al(OH)3↓ |
| B | 由水电离出的H+浓度为1×10-12mol?L-1 | NH4+、Na+、NO3-、Cl- | 一定能大量共存,NH4++H2O?NH3?H2O+H+ |
| C | pH=1的溶液 | Fe2+、Al3+、SO42-、MnO4- | 不能大量共存,5Fe2++MnO4-+8H+═Mn2++5Fe3++4H2O |
| D | 通入少量的SO2气体 | K+、Na+、ClO-、SO42- | 不能大量共存,2ClO-+SO2+H2O═2HClO+SO32- |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com