
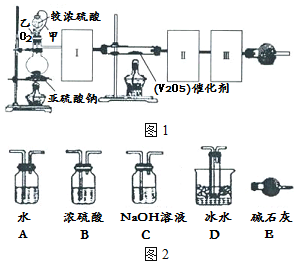
���� ��1��Բ����ƿ���������Ļ�ѧ����ʽΪNa2SO3+H2SO4��Ũ��$\frac{\underline{\;\;��\;\;}}{\;}$Na2SO4+SO2��+H2O����������ĸ�����Ũ���ᣬ���¶ȵ���16.8����Ի����������ľ��壬β���������ռ���Һ��
��2���ȼ��ȴ����ٽ��еμ�Ũ�����������Ϊ��֤���ɵĶ��������ܵ�ת��Ϊ��������
��3������װ�õķ�Һ©���Ͻ���Ƥ�ܼ�Ŀ���DZ��ֺ�ѹ��ʹ��Һ©����Һ��˳�����£�
��4������SԪ���غ�Na2SO3��SO2���������ĵ����ʵ������ɼ���ת���ʣ�
��� �⣺��1��Բ����ƿ���������Ļ�ѧ����ʽΪNa2SO3+H2SO4��Ũ��$\frac{\underline{\;\;��\;\;}}{\;}$Na2SO4+SO2��+H2O��SO2ת����SO3֮ǰ����Զ���������и��������װ��B��Ũ������SO3���۵���16.8�棬�е���44.8�棬���¶ȵ��� 16.8��ʱ��ͨ��װ��D�еı�ˮ��ȴ�����������Ծ���״̬���ڣ������������������β��������װ��C���ռ���Һ���գ���ĸ�������B��D��C��
�ʴ�Ϊ��B��D��C��
��2��Ϊ��֤���ɵĶ��������ܶ��ת��Ϊ��������Ӧ�ȼ��ȴ����ٽ��еμ�Ũ�����������֤���ɵĶ��������ܵIJ��뷴Ӧ��������������װ��I��װ�â�֮�䷢���ķ�Ӧ�Ļ�ѧ����ʽΪ2SO2+O2$\frac{\underline{����}}{��}$2SO3��
�ʴ�Ϊ��2SO2+O2$\frac{\underline{����}}{��}$2SO3��
��3������װ�õķ�Һ©���Ͻ���Ƥ�ܼ�Ŀ���DZ��ֺ�ѹ��ʹ��Һ©����Һ��˳�����£��ʴ�Ϊ�����ֺ�ѹ��ʹ��Һ©����Һ��˳�����£�
��4����126g Na2SO3��ĩ���ʵ���=$\frac{126g}{126g/mol}$=1mol��������Ũ�������ʵ�飬����Ӧ����ʱ������ͨ��O2һ��ʱ�䣬�����װ�â�������51.2g������Ԫ���غ�Na2SO3��SO2����1mol�����ɶ�������1mol��װ�â�������51.2g��˵��ʣ��Ķ�������Ϊ51.2g�����ʵ���=$\frac{51.2g}{64g/mol}$=0.8mol��
���Զ��������ת����=$\frac{1mol-0.8mol}{1mol}$��100%=20%��
�ʴ�Ϊ��20%��
���� ���⿼���˰�����ʵ�����Ʒ��������Ǹ߿��еij������ͣ������е��Ѷȵ����⣻�����ۺ���ǿ�����ض�ѧ��������������ѵ��������������ѧ���淶�Ͻ���ʵ����ơ�����������



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Ca��NO3 ��2����Һ�� | B�� | K2CO3����Һ�� | C�� | CH3COOK�����壩 | D�� | CuSO4 �����壩 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
| A�� | ���³�ѹ�£��ܽ��С�����β�����ת��Ϊ�ܽ����Դ�Щ������ | |
| B�� | ��ͬ�����£�2mol��ԭ�������е�����С��1mol����������е����� | |
| C�� | ��ͬ�����£�1L0.1mol/L��̼������Һ��pH����2L0.1mol/L�Ĵ�������Һ��pH | |
| D�� | 1L 1mol/L��̼������Һ����S02��������1L 1mol/L������Һ����SO2���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��ȥCO2�е�HCl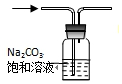 | |
| B�� | �Ʊ�Fe��OH��2���ܽϳ�ʱ��۲�����ɫ | |
| C�� | ��֤̼�������ǿ�ڹ��� | |
| D�� | ���뱽�;ƾ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��һ���������� | B�� | ��ֻ���� S �� N2 | ||
| C�� | ��һ���������� | D�� | ��Ӧ�ڿ����Ƿ�������ԭ��Ӧ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��ƶ���
 ij��A���л���ѧ��ҵ�Ļ���ԭ�ϣ������������������һ�����ҵ�ʯ�ͻ�����չˮƽ��A����һ��ֲ���������ڼ���A�ɷ�����ͼ��ʾ��һϵ�л�ѧ��Ӧ�����Т٢ڢ�����ͬ�ַ�Ӧ���ͣ�
ij��A���л���ѧ��ҵ�Ļ���ԭ�ϣ������������������һ�����ҵ�ʯ�ͻ�����չˮƽ��A����һ��ֲ���������ڼ���A�ɷ�����ͼ��ʾ��һϵ�л�ѧ��Ӧ�����Т٢ڢ�����ͬ�ַ�Ӧ���ͣ� ��
�� ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ͼʾװ�ÿ�������ȡ�۲�Fe��OH��2�ڿ����б�����ʱ����ɫ�仯��ʵ��ʱ����ʹ�õ�ҩƷ����м��6mol•L-1�����ᣬ�����Լ���ѡ��
ͼʾװ�ÿ�������ȡ�۲�Fe��OH��2�ڿ����б�����ʱ����ɫ�仯��ʵ��ʱ����ʹ�õ�ҩƷ����м��6mol•L-1�����ᣬ�����Լ���ѡ���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� |  �����չ� | B�� |  ���ʯ�� | C�� |  ˮ����� | D�� |  Ԥ������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��ƶ���

�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com