

| A. | 装置①可用于分离C2H5OH和H2O的混合物 | |
| B. | 装置②可用于收集H2、Cl2等气体 | |
| C. | 装置③可用于有关NH3实验的尾气处理 | |
| D. | 装置④可用于洗涤BaSO4淀表面吸附的少量氯化钠 |
分析 A.该装置用于分离互不相溶的液体;
B.该装置能收集常温下和空气不反应的气体;
C.氨气极易溶于水,尾气处理要防止倒吸;
D.难溶性固体和溶液采用过滤方法分离.
解答 解:A.水和乙醇互溶,不能采用分液方法分离,应该采用蒸馏方法分离,故A错误;
B.常温下氢气、氯气和空气都不反应,且与空气密度相差较大,所以该装置可用于氢气、氯气等气体,故B正确;
C.倒置的干燥管能防止倒吸,所以该装置可用于有关氨气实验的尾气处理,故C正确;
D.硫酸钡不溶于水,氯化钠易溶于水,所以可以采用过滤方法分离,则装置④可用于洗涤BaSO4淀表面吸附的少量氯化钠,故D正确;
故选A.
点评 本题考查化学实验方案评价,为高频考点,涉及物质分离和提纯、气体收集及尾气处理等知识点,明确实验原理及物质性质、基本实验操作等知识点是解本题关键,注意基本操作规范性,知道常见物质分离和提纯方法,易错选项是C,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 任何气体单质在标准状况下体积约为22.4L,则含有2NA个原子 | |
| B. | 常温常压下,22g氧气和26g臭氧所含氧原子总数为3NA | |
| C. | 常温常压下,11.2L甲烷(CH4)中含有的氢原子数为2NA | |
| D. | 标准状况下,0.3mol二氧化碳中含有氧原子数0.3NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
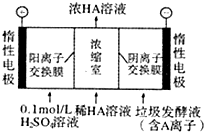 对工业废水和生活污水进行处理是防止水体污染、改善水质的主要措施之一.
对工业废水和生活污水进行处理是防止水体污染、改善水质的主要措施之一.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 它是氧化物 | B. | 它含有3种元素 | ||
| C. | 它的摩尔质量是44 g/mol | D. | 1 mol C2H4O含有2NA个碳原子 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1.0 L 1.0 mo1•L-1的NaAlO2 水溶液中含有的氧原子数为2 NA | |
| B. | 含有NA个原子的氢气在标准状况下的体积约为22.4 L | |
| C. | 标准状况下,2.24 LCl2与足量水反应转移的电子数为0.2NA | |
| D. | V L a mol•L-1的氯化铁溶液中,若Fe3+的数目为NA,则Cl-的数目大于3NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 明矾--Al2(SO4)3•12H2O | B. | 漂白粉--NaClO | ||
| C. | 苏打粉--NaHCO3 | D. | 水煤气--CO、H2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com