
����Ŀ��(1)��ˮɹ�������������ز�֮һ�����к���һ������CH3COOH��д��CH3COOH�ĵ��뷽��ʽ ______�����Ѵ�ƽ���������Һ�м���һ����CH3COONa ������ҺpH_______����������������С����������������
(2)ȼ�ϵ����������������ȼ�ϵ����������ʵ������Ⱦ�����ŷţ�����ϵͳ������������������ȡ֮��������֮����,���ȼ�ϵ��������Ϊ������ҵ��ע�Ľ��㡣ȼ�ϵ�ص�ȼ�Ͽ������������״��ȡ��пƼ�����������ϡ��������������Ϊ��������������˼״�������ȼ�ϵ�ء�����ϡ�������������ڸ������ܴ���O2-��
�ٸõ�ص�������Ӧ��___________��������Ӧ��____________��
����ϡ��������Ĺ��������У�O2-���ƶ�������__________��
�ۼ״���������ȼ����ȼ��ֱ�Ӳ��������ƶ����������У����Ƽ�������Ҫ���Ѵ����ľ����о��״�ȼ������,��Ҫԭ����___________��
(3)��AgCl�ı�����Һ�д��ڳ����ܽ�ƽ�⣺AgCl(s) ![]() Ag+(aq)+Cl-(aq)����25��ʱ,Ksp(AgCl)��1.8��10-10���ֽ������Ȼ����ֱ���룺
Ag+(aq)+Cl-(aq)����25��ʱ,Ksp(AgCl)��1.8��10-10���ֽ������Ȼ����ֱ���룺
��100 mL����ˮ�У���100 mL 0.2 mol/L AgNO3��Һ�У���100 mL 0.1 mol/L�Ȼ�����Һ�У���100 mL 0.1 mol/L�����У���ֽ������ͬ�¶���c(Ag��)�ɴ�С��˳����_____(��д���)�����Т��������ӵ�Ũ��Ϊ______mol/L��
���𰸡�CH3COOH![]() CH3COO-+H+ ���� O2+4e-= 2O2- CH3OH+3O2--6e-=CO2��+2H2O ���������� ȼ�ϵ�ص�����ת���ʸ� �ڢ٢ܢ� 9��10-10
CH3COO-+H+ ���� O2+4e-= 2O2- CH3OH+3O2--6e-=CO2��+2H2O ���������� ȼ�ϵ�ص�����ת���ʸ� �ڢ٢ܢ� 9��10-10
��������
(1)CH3COOH��һԪ���ᣬ����Һ�д��ڵ���ƽ�⣻������Ũ�ȶԵ���ƽ���Ӱ�켰��ҺpH����������
(2)�ڼ״�ȼ�ϵ���ڣ�ͨ��״��ĵ缫Ϊ������ͨ������ĵ缫Ϊ��������������������Ӧ�������Ϸ�����ԭ��Ӧ��������е����������ƶ����������������ƶ���
(3) AgCl�ı�����Һ�д��ڳ����ܽ�ƽ�⣬��Ũ�ȵ�c(Cl-)��c(Ag��)��ƽ���ƶ���Ӱ����ͬ���ɸ���ƽ���ƶ�ԭ��������Һ��c(Ag��)����Դ�С��
(1) CH3COOH��һԪ���ᣬ����Һ�д��ڵ���ƽ�⣺CH3COOH![]() CH3COO-+H+�������Һ�м���CH3COONa���ε��������CH3COO-ʹ��Һ��c(CH3COO-)������ƽ���ƶ�ԭ���������������Ũ�ȣ�pH�����ƶ�����Һ��c(H+)��С�������Һ��pH����
CH3COO-+H+�������Һ�м���CH3COONa���ε��������CH3COO-ʹ��Һ��c(CH3COO-)������ƽ���ƶ�ԭ���������������Ũ�ȣ�pH�����ƶ�����Һ��c(H+)��С�������Һ��pH����
(2)�ٸõ�ص�������Ӧ��O2��õ��ӱ�ΪO2-���缫��ӦʽΪO2+4e-= 2O2-��������CH3OHʧȥ���ӣ��������е�O2-����γ�CO2��ˮ����˸����ĵ缫��Ӧʽ��CH3OH+3O2--6e-=CO2��+2H2O��
����ϡ��������Ĺ��������У�O2-������ɽ϶�ĸ��������ƶ������ƶ������Ǵ�����������
�ۼ״���������ȼ����ȼ��ֱ�Ӳ��������ƶ�����������,���Ƽ�������Ҫ���Ѵ����ľ����о��״�ȼ����������Ҫԭ����ȼ�ϵ�ص�����ת���ʸߣ�
(3)��AgCl�ı�����Һ�д��ڳ����ܽ�ƽ�⣺AgCl(s)![]() Ag+(aq)+Cl-(aq)���������м���AgNO3��Һ����������Һ��Ag+��Ũ�ȣ������ܽ�ƽ�������ƶ������ܵ���˵ƽ���ƶ������������ģ��ﵽƽ�����Һ��c(Ag+)��ˮ�дۼ����Ȼ�����Һ����Һ��c(Cl-)����ƽ�������ƶ����ﵽƽ�����Һ��c(Ag+)�Ȣ��ܽ���ˮ��С�����ܽ���HCl�У�Ҳʹ��Һ��c(Cl-)����ƽ�������ƶ�������c(Cl-)�Ȣ�С�������������ñȢ��������մﵽƽ��ʱ��Һ��c(Ag+)�Ȣ۴�һЩ���ʳ�ֽ������ͬ�¶���c(Ag��)�ɴ�С��˳���Ǣڢ٢ܢۣ�
Ag+(aq)+Cl-(aq)���������м���AgNO3��Һ����������Һ��Ag+��Ũ�ȣ������ܽ�ƽ�������ƶ������ܵ���˵ƽ���ƶ������������ģ��ﵽƽ�����Һ��c(Ag+)��ˮ�дۼ����Ȼ�����Һ����Һ��c(Cl-)����ƽ�������ƶ����ﵽƽ�����Һ��c(Ag+)�Ȣ��ܽ���ˮ��С�����ܽ���HCl�У�Ҳʹ��Һ��c(Cl-)����ƽ�������ƶ�������c(Cl-)�Ȣ�С�������������ñȢ��������մﵽƽ��ʱ��Һ��c(Ag+)�Ȣ۴�һЩ���ʳ�ֽ������ͬ�¶���c(Ag��)�ɴ�С��˳���Ǣڢ٢ܢۣ�
���ڢ�100 mL 0.2 mol/L AgNO3��Һ��c(Ag��)=0.2mol/L������Ksp(AgCl)=1.8��10��10������c(Cl-)= Ksp(AgCl)��c(Ag��)= 1.8��10��10��0.2=9��10-10 mol/L��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������YX2��ZX2�У�X��Y��Z�ĺ˵����С��18��Xԭ�������ܲ��p�ܼ�����һ�����������2�����ӣ�Yԭ�ӵ��������p�ܼ��ĵ���������ǰһ�ܲ������������X��Y������ͬ�ĵ��Ӳ㣻Z��X�����ڱ���λ��ͬһ���塣�ش��������⣺
(1)X�ĵ����Ų�ʽΪ_______��Y�Ĺ����ʾʽΪ_______��
(2)ZX2�ķ���ʽ��_______��YX2����ʽ��_________��
(3)Y��Z�γɵĻ�����ķ���ʽ��_______��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��ѧС�鹹�뽫����β��(NO��NO2)ת��Ϊ��Ҫ�Ļ���ԭ��HNO3����ԭ����ͼ��ʾ������A��BΪ��ײ��ϡ�����˵����ȷ���ǣ� ��

A. �������Һ�е����ķ�����B��A
B. �缫B������c(NO3��)����
C. �缫A���淴Ӧ֮һΪNO��2H2O��3e��===NO3����4H��
D. �õ�ع���ʱ��ÿת��4 mol���ӣ�����22.4 L O2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����й��ڱ���������ȷ����
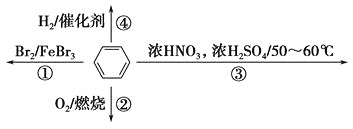
A. ��Ӧ��Ϊȡ����Ӧ���л�������ˮ��ϸ����ϲ�
B. ��Ӧ��Ϊ������Ӧ����Ӧ�����ǻ�������������Ũ��
C. ��Ӧ��Ϊȡ����Ӧ���л�������һ����
D. ��Ӧ����1 mol�������3 mol H2�����ӳɷ�Ӧ����Ϊÿ�������Ӻ�������̼̼˫��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��(1)�������ȡ����Ӧ��ʵ��װ����ͼ��ʾ������AΪ��֧�Թܸ��Ƴɵķ�Ӧ�����������¶˿���һС�ף�����ʯ���ޣ��ټ���������м��

��д���пհף�
���Թ�A�еķ�Ӧ����ʽΪ______________��
���Թ�C�����Ȼ�̼�������ǣ�____________________________����Ӧ��ʼ�۲�D�Թܣ�����������Ϊ��_______________��д��E�з�Ӧ�����ӷ���ʽ______________��
�۷�Ӧ2��3 min����B�е�NaOH��Һ��ɹ۲쵽��������____________��
������������װ���У����з��������ܵ�������________(����ĸ)��
(2)ʵ�����Ʊ�����������Ҫ�������£�
a������һ��������ŨH2SO4��ŨHNO3�Ļ���ᣬ���뷴Ӧ���У�
b���������µĻ��������μ���һ�����ı����������Ͼ��ȣ�
c����55��60 ���·�����Ӧ��ֱ����Ӧ������
d����ȥ�����ֲ�Ʒ����������ˮ��5%NaOH��Һϴ�ӣ������������ˮϴ�ӣ�
e��������ˮCaCl2�����Ĵ��������������õ�����������������д���пհף�
���Ʊ��������ķ�Ӧ������________��
������һ��������ŨH2SO4��ŨHNO3�Ļ����ʱ��������ע�������ǣ�_____________��
�۲���d��ϴ�ӡ������������Ӧʹ�õ�������_________________��
�ܲ���d�дֲ�Ʒ��5%NaOH��Һϴ�ӵ�Ŀ����___________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������ijЩ���������˲�ͬ�̶ȵ�������������У����С���ͬѧ��������˵����о�,
��.����С���о�����,������Ҫ��Ⱦ��Ϊ�����������PM2.5������Ҫ��ԴΪȼú��������β���ȡ�
(1)25��ʱ��PM2.5����������ˮ�����Ƴɴ�����Һ����ø���������ˮ���������ӵĻ�ѧ��ּ���ƽ��Ũ�����±���

���ݱ��������ж�������pH=________��
��.���������������������һ���о�
һ�������������������о�
(1)һ�������£���2molNO��2molO2���ں����ܱ������з�����Ӧ��
2NO(g)+O2(g) ![]() 2NO2(g)������״̬��˵���÷�Ӧ�ﵽ��ѧƽ�����_______������ĸ��ţ���
2NO2(g)������״̬��˵���÷�Ӧ�ﵽ��ѧƽ�����_______������ĸ��ţ���
A�����������ܶȱ��ֲ��� B��NO��ת���ʱ��ֲ���
C��NO��O2�����ʵ���֮�ȱ��ֲ��� D��O2���������ʺ�NO2�������������
(2)����̿�ɴ���������Ⱦ��NO����Ӧԭ��Ϊ��C(s)+2NO(g)![]() N2(g)+CO2(g)��T��ʱ����2L�ܱ������м���0.100mol NO��2.030mol����̿�������ʣ���ƽ��ʱ����̿���ʵ�����2.000mol������¶��µ�ƽ�ⳣ��Ϊ_________����ƽ��ʱ,�����������г���0.04molNO,0.03molN2��0.03molCO2����ƽ��________�ƶ���������������������������������
N2(g)+CO2(g)��T��ʱ����2L�ܱ������м���0.100mol NO��2.030mol����̿�������ʣ���ƽ��ʱ����̿���ʵ�����2.000mol������¶��µ�ƽ�ⳣ��Ϊ_________����ƽ��ʱ,�����������г���0.04molNO,0.03molN2��0.03molCO2����ƽ��________�ƶ���������������������������������
III.һ����̼��������̼���о�
(1)CO��CO2��һ�������¿��������ϳɼ״�����ҵ�ϳ���CO��H2�Ʊ�CH3OH�ķ�ӦΪ��CO(g)+2H2(g)![]() CH3OH(g)�������Ϊ1L�ĺ����ܱ������У�����2molCO��4molH2��һ�������·���������Ӧ�����CO(g)��CH3OH(g)��Ũ����ʱ��仯��ͼ��ʾ���ӷ�Ӧ��ʼ��5min����H2��ʾ��ƽ����Ӧ����v(H2)=_____��
CH3OH(g)�������Ϊ1L�ĺ����ܱ������У�����2molCO��4molH2��һ�������·���������Ӧ�����CO(g)��CH3OH(g)��Ũ����ʱ��仯��ͼ��ʾ���ӷ�Ӧ��ʼ��5min����H2��ʾ��ƽ����Ӧ����v(H2)=_____��

(2)̼��ˮ������Ӧ��ȡH2����ط�Ӧ���£�
��C(s)+H2O(g)=CO(g)+H2(g) �� H=+131.0kJ/mol
��CO(g)+H2O(g)=CO2(g)+H2(g) �� H= - 43kJ/mol
��CaO(s)+CO2(g)=CaCO3(S) �� H= - 178.3kJ/mol
�ټ��㷴Ӧ����C(s)+2H2O(g)+CaO(s)![]() CaCO3(s)+2H2(g)����H=______kJ/mol��
CaCO3(s)+2H2(g)����H=______kJ/mol��
�������������о�
��SO2�ɱ�Na2FeO4������ȥ����Ⱦ����ҵ����Fe��ʯī���缫���ŨNaOH��Һ�Ʊ�Na2FeO4��д�������������������ĵ缫��Ӧ________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������ӵ�VSEPRģ���������幹��һ�µ���(����)
A. SO![]() B. ClO
B. ClO![]() C. NO
C. NO![]() D. ClO
D. ClO![]()
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Ԫ�����ڱ���ǰ�����ڲ���Ԫ�ص�ԭ�������볣����̬�Ĺ�ϵͼ���¡�����ԭ��������ʾ��ӦԪ�أ�����˵���в���ȷ����

A.a��d�ķǽ����ԱȽϣ�a> d
B.ԭ�Ӱ뾶��С��b>c>a>d>e
C.a�����γ������⻯��
D.b��c��e������������Ӧˮ����֮����ɷ�Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����������£�![]() ��
��![]() �����ʵ���
�����ʵ���![]() ǡ����ȫ��Ӧ�����ɵIJ�����ʹ������Һ������������������ӷ���ʽ���������ƽ��
ǡ����ȫ��Ӧ�����ɵIJ�����ʹ������Һ������������������ӷ���ʽ���������ƽ��
��________��H++��________��NO2-+��________��I-����_________��+��__________��+��__________��H2O
�����������ӷ���ʽ��1Ħ��![]() ���뷴Ӧ��ת�Ƶĵ�����Ŀ��______����Ӧ�б���ԭ��Ԫ����______��
���뷴Ӧ��ת�Ƶĵ�����Ŀ��______����Ӧ�б���ԭ��Ԫ����______��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com