
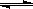 HCO3££«OH-£Ø2·Ö£©
HCO3££«OH-£Ø2·Ö£©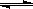 HCO3££«OH-”£¼ÓČėĀČ»Æ±µČÜŅŗ£¬Ba2+»įŗĶCO32£·“Ó¦£¬Ź¹Ė®½ā·“Ó¦ÄęĻņŅĘ¶Æ£¬¼īŠŌ¾Ķ¼õČõ£¬ŃÕÉ«¾ĶĶĖČ„”£
HCO3££«OH-”£¼ÓČėĀČ»Æ±µČÜŅŗ£¬Ba2+»įŗĶCO32£·“Ó¦£¬Ź¹Ė®½ā·“Ó¦ÄęĻņŅĘ¶Æ£¬¼īŠŌ¾Ķ¼õČõ£¬ŃÕÉ«¾ĶĶĖČ„”£


| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗŹµŃéĢā

²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
 ”¢¢Ś100ml 0.1 mol/L
”¢¢Ś100ml 0.1 mol/L  Į½ÖÖČÜŅŗµÄŠšŹö²»ÕżČ·µÄŹĒ£Ø
Į½ÖÖČÜŅŗµÄŠšŹö²»ÕżČ·µÄŹĒ£Ø | A£®¢ŁČÜŅŗÖŠ:c(CO32£)> c(H2CO3) | B£®ČÜŅŗÖŠŅõĄė×ÓµÄĪļÖŹµÄĮæÅضČÖ®ŗĶ:¢Ś>¢Ł |
C£®ČÜŅŗÖŠĖ®µēĄė³öµÄ øöŹż£ŗ¢Ś>¢Ł øöŹż£ŗ¢Ś>¢Ł | D£®¢ŚČÜŅŗÖŠ: c(HCO3£)> c(H2CO3) |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
| A£®V£ØNaOH£©£½0Ź±£¬c(H+)£½1”Į10-2 mol/L |
| B£®V£ØNaOH£©£½10 mLŹ±£¬c(H+)£½1”Į10-7 mol/L |
C£®V£ØNaOH£©£¼10 mLŹ±£¬æÉÄÜ“ęŌŚc(Na+)£½ |
D£®V£ØNaOH£©£¾10 mLŹ±£¬ £¾ £¾ £¾ £¾ ) ) |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗŹµŃéĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
| A£®µČĮæµÄĮņÕōĘųŗĶĮņ¹ĢĢå·Ö±šĶźČ«Č¼ÉÕ£¬ŗóÕ߷ųöČČĮæ¶ą |
| B£®ÓÉC(ŹÆÄ«)”śC(½šøÕŹÆ)¦¤H =" +119" kJ”¤mol”Ŗ1æÉÖŖ£¬ŹÆÄ«±Č½šøÕŹÆĪČ¶Ø |
| C£®Éś³ÉĪļÖŠČ«²æ»Æѧ¼üŠĪ³ÉŹ±ĖłŹĶ·ÅµÄÄÜĮæ“óÓŚĘĘ»µ·“Ó¦ĪļÖŠČ«²æ»Æѧ¼üĖłĪüŹÕµÄÄÜĮæŹ±£¬·“Ó¦ĪŖĪüČČ·“Ó¦ |
| D£®ŌŚ101 kPaŹ±£¬2g H2ĶźČ«Č¼ÉÕÉś³ÉŅŗĢ¬Ė®£¬·Å³ö285.8 kJČČĮ棬Ōņ±ķŹ¾ĒāĘųČ¼ÉÕČȵÄČČ»Æѧ·½³ĢŹ½ĪŖ2H2£Øg£©+ O2£Øg£©= 2H2O£Øl£© ¦¤H = ”Ŗ285.8 kJ”¤ mol”Ŗ1 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
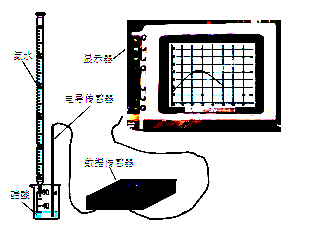
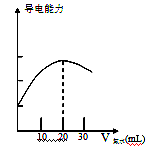
 Ba2++2OH-Ļņ“ĖÖÖŠü×ĒŅŗÖŠ¼ÓČėÉŁĮæµÄĒāŃõ»Æ±µ·ŪÄ©£¬ĻĀĮŠŠšŹöÕżČ·µÄŹĒ
Ba2++2OH-Ļņ“ĖÖÖŠü×ĒŅŗÖŠ¼ÓČėÉŁĮæµÄĒāŃõ»Æ±µ·ŪÄ©£¬ĻĀĮŠŠšŹöÕżČ·µÄŹĒ| A£®ČÜŅŗÖŠ±µĄė×ÓŹżÄæ¼õŠ” |
| B£®ČÜŅŗÖŠ±µĄė×ÓÅØ¶Č¼õŠ” |
| C£®ČÜŅŗÖŠĒāŃõøłĄė×ÓÅضČŌö“ó |
| D£®pHÖµ¼õŠ” |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com