
下列事实不能用元素周期律解释的是
A.向Na2SO3溶液中加盐酸,有气泡产生
B.0.1 mol•L-1溶液的pH:NaOH>LiOH
C.Mg、Al与同浓度盐酸反应,Mg更剧烈
D.气态氢化物的稳定性:HBr>HI
科目:高中化学 来源:2015-2016学年安徽黄山屯溪一中高一下期中化学试卷(解析版) 题型:选择题
X和Y是短周期元素,二者能形成化合物X2Y3,若Y的原子序数为n,则X的原子序数不可能是
A.n﹣8 B.n﹣3 C.n﹣1 D.n+5
查看答案和解析>>
科目:高中化学 来源:2016届西藏日喀则一中高三下学期二模考试理综化学试卷(解析版) 题型:选择题
25℃时,c(CH3COOH)+c(CH3COO-)=0.1mol•L-1的醋酸、醋酸钠混合溶液中,c(CH3COOH)、c(CH3COO-)与pH的关系如图所示.下列叙述正确的是( )
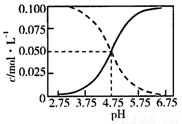
A.25℃时,CH3COOH的电离常数K的值5×10-2.75
B.随pH增大, 增大
增大
C.pH=4的溶液中,c(CH3COO-)>c(CH3COOH)>c(H+)>c(OH-)
D.pH=5的溶液中,c(H+)+c(Na+)+c(CH3COOH)-c(OH-)=0.1 mol•L-1
查看答案和解析>>
科目:高中化学 来源:2016届山西省高三第二轮训练三化学试卷(解析版) 题型:选择题
下列说法不正确的是
A.Na与H2O的反应是熵增的放热反应,该反应能自发进行
B.饱和Na2SO3溶液或浓硝酸均可使蛋白质溶液产生沉淀,但原理不同
C.FeCl3和MnO2均可加快H2O2分解,同等条件下二者对H2O2分解速率的改变相同
D.Mg(OH)2固体在溶液中存在平衡:Mg(OH)2(s)  Mg2+(aq)+2OH-(aq),该固体可溶于NH4Cl溶液
Mg2+(aq)+2OH-(aq),该固体可溶于NH4Cl溶液
查看答案和解析>>
科目:高中化学 来源:2016届宁夏六盘山高中高三第四次模拟理综化学试卷(解析版) 题型:选择题
下列各溶液中,微粒的物质的量浓度关系表述正确的是
A.0.1 mol/LNa2CO3溶液中:c(Na+)=(HCO3-)+c(H2CO3)+2c(CO32-)
B.pH=l2的Ba(OH)2溶液和pH=12的Na2CO3溶液中,水电离的c(H+)相等
C.将0.2mol/LNaA溶液和0.1 mol•L-1盐酸溶液等体积混合所得碱性溶液中:c(Na+)+c(H+)=c(A-)+c(Cl-)
D.常温下pH=4的醋酸与pH=10的NaOH溶液等体积混合后pH<7
查看答案和解析>>
科目:高中化学 来源:2016届内蒙古赤峰二中高三第四次模拟理综化学试卷(解析版) 题型:填空题
冬季是雾霾天气高发的季节,其中汽车尾气和燃煤尾气是造成雾霾的原因之一.
(1)汽车尾气净化的主要原理为:2NO(g)+2CO(g)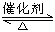 2CO2(g)+N2(g)
2CO2(g)+N2(g)
①一定条件下,在一个容积固定为2L的密闭容器中充入0.8mol NO和1.2mol CO,开始反应至2min时测得CO转化率为20%,则用N2表示的平均反应速率为v(N2)=_________。
②对于气相反应,用某组分(B)的平衡压强(PB)代替物质的量浓度(CB)也可以表示平衡常数(记作KP),则该反应平衡常数的表达式KP=_________。
③该反应在低温下能自发进行,该反应的△H_________0(填“>”、“<”)
④在某一绝热、恒容的密闭容器中充入一定量的NO、CO发生上述反应,测得正反应的速率随时间变化的曲线如图所示(已知:t2-t1=t3-t2)则下列说法不正确的是_________(填编号)
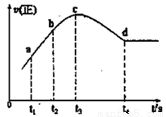
A.反应在c点未达到平衡状态
B.反应速率a点小于b点
C.反应物浓度a点大于b点
D.NO的转化率:t1~t2>t2~t3
(2)使用甲醇汽油可以减少汽车尾气对环境的污染.某化工厂用水煤气为原料合成甲醇,恒温条件下,在体积可变的密闭容器中发生反应CO(g)+2H2(g)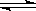 CH3OH(g)到达平衡时,测得CO、H2、CH3OH分别为1mol、1mol、1mol,容器的体积为3L,现往容器中继续通入3mol CO,此时v(正)_________v(逆)(填“>”、“<”或“=”),判断的理由_________。
CH3OH(g)到达平衡时,测得CO、H2、CH3OH分别为1mol、1mol、1mol,容器的体积为3L,现往容器中继续通入3mol CO,此时v(正)_________v(逆)(填“>”、“<”或“=”),判断的理由_________。
(3)二甲醚也是清洁能源.用合成气在催化剂存在下制备二甲醚的反应原理为:2CO(g)+4H2(g)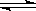 CH3OCH3(g)+H2O(g),已知一定条件下,该反应中CO的平衡转化率随温度、投料比
CH3OCH3(g)+H2O(g),已知一定条件下,该反应中CO的平衡转化率随温度、投料比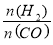 的变化曲线如图:
的变化曲线如图:
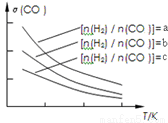
①a、b、c按从大到小的顺序排序为_________。
②某温度下,将某温度下,将2.0molCO(g)和6.0molH2(g)充入容积为2L的密闭容器中,反应到达平衡时,改变压强和温度,平衡体系中CH3OCH3(g)的物质的量分数变化情况如图3所示,关于温度和压强的关系判断正确的是_________
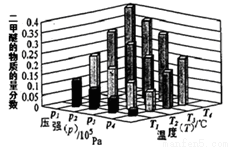
A.P3>P2,T3>T2B.P1>P3,T1>T3
C.P2>P4,T4>T2D.P1>P4,T2>T3
③在恒容密闭容器里按体积比为1:3充入一氧化碳和氢 气,一定条件下反应达到平衡状态.当改变反应的某一个条件后,下列变化能说明平衡一定向逆反应方向移动的是_________
A.正反应速率先增大后减小 B.逆反应速率先增大后减小
C.化学平衡常数K值增大 D.反应物的体积百分含量增大
E.混合气体的密度减小 F.氢气的转化率减小.
查看答案和解析>>
科目:高中化学 来源:2016届内蒙古赤峰二中高三第四次模拟理综化学试卷(解析版) 题型:选择题
下列说法正确的是
A.把SO2通入酸性高锰酸钾溶液,即可验证SO2的漂白性
B.无论是在0.1mol•L-1的CH3COOH溶液中加水稀释,还是加入少量CH3COONa晶体,都会引起溶液的导电能力减弱
C.实验室需用480mL 0.1mol•L-1硫酸铜溶液,应称取12.5g胆矾晶体,并用500mL容量瓶定容配制
D.硫酸亚铁铵晶体中NH4+的检验操作为:取适量样品置于试管中加水溶解,滴加少量稀氢氧化钠溶液,并将湿润的红色石蕊试纸靠近试管口,试纸变蓝则存在NH4+,反之则不存在NH4+
查看答案和解析>>
科目:高中化学 来源:2015-2016学年四川省高一下期中化学试卷(解析版) 题型:选择题
X、Y、Z三种元素原子的核电荷数在10~18之间,它们的最高价氧化物对应水化物是HXO4、H2YO4、H3ZO4。则下列判断正确的是( )
A.非金属性:X<Y<Z
B.含氧酸的酸性:H3ZO4>H2YO4>HXO4
C.原子半径:按X、Y、Z变小
D.气态氢化物稳定性:按X、Y、Z顺序减弱
查看答案和解析>>
科目:高中化学 来源:2015-2016学年河北省高二下期中化学试卷(解析版) 题型:选择题
利用LiOH可制备锂离子电池正极材料。LiOH可由电解法制备,如右图,两极区电解质溶液分别为LiOH和LiCl溶液。下列说法错误的是
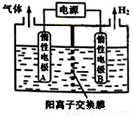
A.B极区电解质溶液为LiOH溶液
B.阳极电极反应式为2Cl--2e-=Cl2↑
C.电解过程中主要是H+通过阳离子交换膜向B电极迁移
D.电极A连接电源的正极
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com