
【题目】KClO3和浓盐酸在一定温度下反应会生成黄绿色的易爆物二氧化氯。其变化可表述为: 2KClO3 +4HCl(浓)=2KCl+2ClO2↑+Cl2↑+2H2O。
(1)请分析该反应中电子转移的情况:(单线桥法表示)________________________。
(2)氧化剂与还原剂的物质的量之比是 ___________________
(3)若产生标况下22.4 L Cl2,则转移的电子的物质的量为________mol。
(4)实验室备用的浓盐酸质量分数为36.5%,密度为1.19 g·cm-3,为使用方便,请计算出该浓盐酸中HCl的物质的量浓度 mol·L-1。
(5)ClO2对污水中Fe2+、Mn2+、S2-和CN- 等有明显的去除效果。某工厂污水中含CN- a mg/L,现用ClO2将CN - 氧化,只生成两种气体,其离子反应方程式为为 ,处理100 m3这种污水,至少需要ClO2 _______mol。
【答案】(1)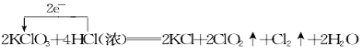 ;
;
(2)1:1;(3)2;(4)11.9;
(5)2ClO2 + 2CN- = N2 + 2CO2 + 2Cl-,50a/13 (或3.85a)。
【解析】
试题分析:(1)根据氧化还原反应中的价态归中规律判断元素化合价只靠拢不交叉,所以氯酸钾中的氯元素化合价由+5降到二氧化氯中的+4价,盐酸中的氯元素由-1价升到0价,该反应中电子转移的情况为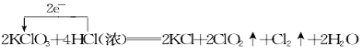 。
。
(2)2mol氯酸钾中的氯元素化合价全部由+5降到二氧化氯中的+4价,作氧化剂,4molHCl中的氯元素的化合价只有2mol由-1价升到0价,作还原剂,氧化剂与还原剂的物质的量之比是1:1。
(3)标况下22.4 L Cl2的物质的量为1mol,根据(1)知转移的电子的物质的量为2mol。
(4)根据公式c=![]() 计算质量分数为36.5%,密度为1.19 g·cm-3的浓盐酸中HCl的物质的量浓度为(1000×1.19×36.5%)÷36.5=11.9mol·L-1。
计算质量分数为36.5%,密度为1.19 g·cm-3的浓盐酸中HCl的物质的量浓度为(1000×1.19×36.5%)÷36.5=11.9mol·L-1。
(5)根据题意知ClO2将CN - 氧化生成二氧化碳和氮气,本身被还原为Cl-,利用化合价升降法配平,该反应的离子方程式为2ClO2 + 2CN- = N2 + 2CO2 + 2Cl- ,废水中CN- 的浓度为a mg/L,即为ag/m3,100 m3污水含CN-的质量为100ag,物质的量为100ag÷26g/mol=50a/13mol,根据反应方程式知至少需要ClO2 50a/13mol 。


 第三学期赢在暑假系列答案
第三学期赢在暑假系列答案 学练快车道快乐假期暑假作业新疆人民出版社系列答案
学练快车道快乐假期暑假作业新疆人民出版社系列答案科目:高中化学 来源: 题型:
【题目】小明用蜡烛进行了下列活动.
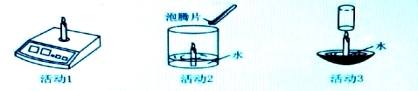
(1)活动1:点燃蜡烛后,电子秤示数逐渐减小.蜡烛减小的质量 (填“大于”、
“等于”或“小于”)燃烧后生成物的总质量.
(2)活动2:加入泡腾片(主要成分含柠檬酸、碳酸氢钠等),观察到水中产生大量气泡、
蜡烛逐渐熄灭.产生上述现象的原因是 。
(3)活动3:用玻璃杯迅速扣住燃烧的蜡烛,并使杯口始终浸没在水中.下列说法正确的
是 (填序号).
A.可观察到蜡烛熄灭 B.最终杯中液面高于碗中液面
C.该方法能准确测定空气中氧气的含量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学反应可视为旧键断裂和新键形成的过程。化学键的键能是形成(或拆开) 1mol化学键时释放(或吸收)的能量。已知白磷(P4)和P4O6的分子结构如下图所示;现提供以下化学键的键能: P-P 198 kJ.mol-1、P-O 360 kJ.mol-1、氧气分子内氧原子间的键能为498 kJ.mol-1 。则P4+3O2 =P4O6的反应热H为
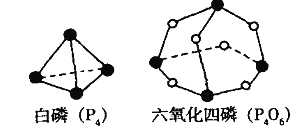
A.+1638 kJ.mol-1 B.-1638 kJ.mol-1
C.-126 kJ.mol-1 D.+126 kJ.mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(27分)
(1)甲烷和氯气发生的一系列反应都是 ______反应,写出第一步反应的化学方程式 ____________________________________________。
(2)分子中含有34个氢原子的烷烃是 ______(填名称),乙烯的结构简式为_____________________,糖尿病患者尿液中含的糖类的分子式 。
(3)现有四种试剂:A.新制的Cu(OH)2;B.浓硝酸;C.AgNO3溶液;D.碘水。为了鉴别下列四瓶无色溶液,请你选择合适的试剂,将其填入相应的括号中。
①葡萄糖溶液( ) ②食盐溶液( )
③淀粉溶液( ) ④鸡蛋清溶液( )
(4)将下列各组金属与其对应的最佳冶炼方法用线连起来:
金属组 冶炼方法
Fe、Zn、Cu等中等活泼的金属 利用铝热反应原理用Al还原
Na、Mg、Al等活泼金属 以C、CO或 H2 作还原剂还原
Hg、Ag等不活泼金属 电解法
V、Cr、Mn、W等高熔点金属 热分解法
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】800 ℃时,向容积为2 L的密闭容器中充入一定量的CO和H2O维持恒温,发生反应CO(g)+H2O(g)![]() H2(g)+CO2(g),反应过程中测定的部分数据见下表:
H2(g)+CO2(g),反应过程中测定的部分数据见下表:
反应时间/min | 0 | 2 | 4 | 6 |
n(CO)/mol | 1.20 | 0.90 | 0.80 | |
n(H2O)/mol | 0.60 | 0.20 |
(1)反应在2 min内的平均速率为v(H2O)=________。
(2)800 ℃时,化学平衡常数K的值为________。
(3)保持其他条件不变,向平衡体系中再通入0.20 mol H2O,与原平衡相比,达到新平衡时CO转化率________(填“增大”、“减小”或“不变”)。
(4)在恒温恒压密闭容器中通入CO和H2O各1 mol发生该反应,当反应达到平衡后,维持温度与压强不变,t1时再通入各1 mol的CO和H2O的混合气体,请在下图中画出正(v正)、逆(v逆)反应速率在t1后随时间t变化的曲线图。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用价层电子对互斥理论预测H2S和PCl3的立体结构,两个结论都正确的是( )
A.直线形;三角锥形
B.V形;三角锥形
C.直线形;平面三角形
D.V形;平面三角形
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关SO2的说法中,不正确的是
A.溶于水能导电,属于电解质
B.使品红溶液褪色,有漂白性
C.使酸性高锰酸钾溶液褪色,有还原性
D.能杀菌、消毒,可按照国家标准用作食物的防腐剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】分子式为C5H7Cl的有机物,其结构不可能是( )
A.只含有1个双键的直链有机物
B.含2个双键的直链有机物
C.含1个双键的环状有机物
D.含一个三键的直链有机物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某气态烃A在标准状况下的密度为1.25g/L,其产量可以用来衡量一个国家的石油化工发展水平。B和D都是生活中常见的有机物,D能跟碳酸氢钠反应,F有香味。它们之间的转化关系如下图所示:
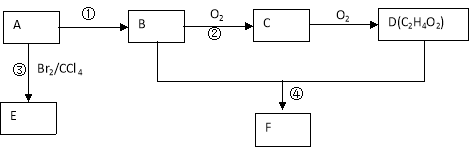
(1)A的结构式为 , D中官能团的名称为 。
(2)反应①的反应类型是 ,反应③的化学方程式为 。
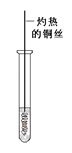
(3)反应②在Cu做催化剂的条件下进行,该实验的步骤是将红亮的铜丝置于酒精灯上加热,待铜丝变为黑色时,迅速将其插入到装有B的试管中(如右上图所示)。重复操作2-3次,观察到的现象是__________。该反应的化学方程式为 。
(4)D与碳酸氢钠溶液反应的离子方程式为 。
(5)B、D在浓硫酸的作用下实现反应④,实验装置如右图所示:
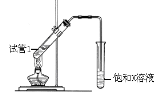
图中X的化学式为_________。浓硫酸的作用是 。
试管Ⅰ中在加热前应加_______,防止液体暴沸。导管末端为伸入小试管液面下的原因是__________。该反应的化学方程式为 。分离产物F的方法是__________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com