
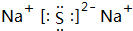 .
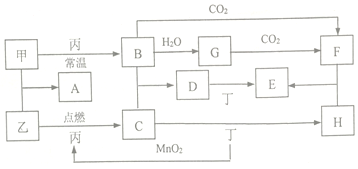
.分析 B的焰色反应为黄色,能与水、二氧化碳反应,则B为Na2O,甲为Na,G为NaOH,F为Na2CO3,丙为O2,C能使品红溶液褪色,应为SO2,则乙为S,由转化关系可知D为Na2SO3,A为Na2S,丁可与二氧化锰反应生成氧气,可知丁为H2O2,E为Na2SO4,H为H2SO4,以此解答该题.
解答 解:(1)由以上分析可知丙为O2,E为Na2SO4,故答案为:O2;Na2SO4;
(2)A为Na2S,电子式为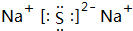 ,故答案为:
,故答案为: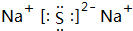 ;
;
(3)B为Na2O,与水反应生成NaOH,方程式为Na2O+H2O=2NaOH,二氧化硫和过氧化氢反应生成硫酸,离子方程式为SO2+H2O2=2H++SO42-,
故答案为:Na2O+H2O=2NaOH;SO2+H2O2=2H++SO42-.
点评 本题考查无机物推断,为高考常见题型,侧重考查学生的分析能力以及元素化合物知识的综合理解和运用,注意把握物质的性质、转化关系中特殊转化等推断突破口,需要学生熟练掌握元素化合物知识,难度中等.


科目:高中化学 来源: 题型:选择题
| A. | 用胆矾炼铜、烧结粘土制陶瓷都涉及化学变化 | |
| B. | 中国古代利用明矾溶液的酸性清除铜镜表面的铜锈 | |
| C. | 食盐、醋酸、氨水和硫酸钡都是电解质 | |
| D. | 胶体区别其它分散系的本质特征是分散质微粒直径在lnm〜l00nm之间 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | SiO2不溶于水,因此不属于酸性氧化物 | |
| B. | CO2通入水玻璃中可得硅酸,说明碳酸酸性大于硅酸 | |
| C. | SiO2是酸性氧化物,它不溶于任何酸 | |
| D. | SiO2晶体由SiO2分子构成,1个Si原子连接2个O原子 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:推断题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com