
CuCl2��Һ�к�����������FeCl2��Ϊ�Ʊ�������CuCl2��2H2O���壬�ⶨʵ�鲽������ͼ��ʾ��
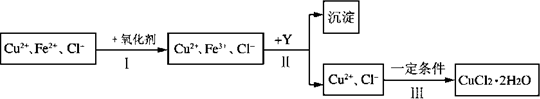
��ش��������⣺
(1)������У���Fe2+ת��ΪFe3+���ѡ�������������е�________(����ĸ)��
A��K2Cr2O7��B��NaClO��C��H2O2
�÷�Ӧ�����ӷ���ʽΪ________��
(2)�ڲ�����У��ټ���Y��Ŀ����Ϊ�˵�����Һ������Դ�ʹFe3+������ȫ��Y���������������е�________(����ĸ)��
A��NaOH��B��Cu��C��Cu2(OH)2CO3
�ڽ����뺣�ڴ����γ�ɳ��ԭ���ǽ�ˮ�еĽ�������ˮ�еĵ���ʷ������ۣ���������г����Ƴɽ��������μ���ϡ������ܿ�����������________��
(3)�����Ӧ���Ƶ�ʵ��������________��

| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| O | 2- 3 |
| O | 2- 6 |
| ���� | Cu��OH��2 | Fe��OH��3 | CuCl | CuI |
| Ksp | 2.2��10-20 | 2.6��10-39 | 1.7��10-7 | 1.3��10-12 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| S2O | 2- 3 |
| S4O | 2- 6 |
| ���� | Cu��OH��2 | Fe��OH��3 | CuCl | CuI |
| Ksp | 2.2��10-20 | 2.6��10-39 | 1.7��10-7 | 1.3��10-12 |
| ||
| ||
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| ���� | Cu��OH��2 | Fe��OH��3 | CuS | PbS | MnS |
| Ksp | 2.2��10-20 | 2.6��10-39 | 6.3��10-36 | 8��10-28 | 2��10-10 |
| ||
| ||
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| ���� | Cu��OH��2 | Fe��OH��3 | CuCl | CuI |
| Ksp | 2.2��10-20 | 2.6��10-39 | 1.7��10-7 | 1.3��10-12 |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com