
【题目】下列有关硫及其化合物的说法中正确的是( )
A.浓硫酸与灼热的炭反应,体现了浓硫酸的强氧化性和酸性
B.浓硫酸具有吸水性,可做干燥剂,不能干燥 NH3、 H2S等气体
C.SO2 和 Cl2 均可使品红溶液褪色,但将溶有 SO2 的品红溶液加热后又恢复红色,说明 SO2 的氧化性没有 Cl2 强
D.以 FeS和稀硫酸反应制H2S气体为氧化还原反应
【答案】B
【解析】
A.浓硫酸与灼热的炭反应,炭被氧化成![]() ,浓硫酸被还原成SO2,体现了硫酸的强氧化性,但是反应产物中没有硫酸盐,因此无法体现硫酸的酸性,A项错误;
,浓硫酸被还原成SO2,体现了硫酸的强氧化性,但是反应产物中没有硫酸盐,因此无法体现硫酸的酸性,A项错误;
B.由于浓硫酸具有酸性和强氧化性,浓硫酸不能干燥碱性气体(如NH3)和还原性气体(如H2S、HI等),B项正确;
C.二氧化硫的漂白原理与氯气的漂白原理不一样,二氧化硫漂白的原理是二氧化硫与有色物质化合成不稳定的无色物质,因此不能根据二氧化硫的漂白是可逆的这一点来判断二者的氧化性强弱,C项错误;
D.![]() 中硫的化合价为-2价,
中硫的化合价为-2价,![]() 中硫的化合价也是-2价,则FeS与稀硫酸发生复分解反应制备H2S,没有元素化合价的变化,因此不是氧化还原反应,D项错误;
中硫的化合价也是-2价,则FeS与稀硫酸发生复分解反应制备H2S,没有元素化合价的变化,因此不是氧化还原反应,D项错误;
答案选B。


科目:高中化学 来源: 题型:
【题目】下图①②③④表示由不同化学元素组成的化合物,以下说法正确的是

A. 若①为某生物大分子的组成单位,则①最可能是核苷酸
B. 若②是细胞中的储能物质,则②一定是脂肪
C. 若③是病毒的遗传物质,则③一定是RNA
D. 若④是植物细胞壁的主要成分,则④可能是纤维素
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某研究性学习小组利用H2C2O4溶液和酸性KMnO4溶液的反应探究“外界条件的改变对化学反应速率的影响”,进行了如下实验:
实验序号 | 实验 温度/K | 有关物质 | 溶液颜色褪至无色所需时间/s | ||||
酸性KMnO4溶液 | H2C2O4溶液 | H2O | |||||
V/mL | c/ mol·L-1 | V mL | c/ mol·L-1 | V/mL | |||
A | 293 | 2 | 0.02 | 4 | 0.1 | 0 | t1 |
B | T1 | 2 | 0.02 | 3 | 0.1 | V1 | 8 |
C | 313 | 2 | 0.02 | V2 | 0.1 | 1 | t2 |
(1)其中V1=_____、T1=_____;通过实验_____(填实验序号)可探究出温度变化对化学反应速率的影响,其中V2=______。
(2)若t1<8,则由此实验可以得出的结论是_____;忽略溶液体积的变化,利用实验B中数据计算,0~8s内,用KMnO4的浓度变化表示的反应速率v(KMnO4)=_______。
(3)该小组的一位同学通过查阅资料发现,上述实验过程中n(Mn2+)随时间的变化情况如图所示,并认为造成这种变化的原因是反应体系中的某种粒子对KMnO4与草酸之间的反应有某种特殊作用,则该作用是_______。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于相同温度、相同压强下,相同物质的量的SO2和SO3,下列说法中正确的是( )
A.硫元素的质量比为5:4B.质量之比为1:1
C.分子数之比为5:4D.密度之比为4:5
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在下列条件的溶液中,各组离子一定能够大量共存的是( )
A.使酚酞溶液变红的溶液:Na+、Cl-、SO42-、Fe3+
B.无色透明溶液中:K+、SO42-、MnO4-、H+
C.含有大量OH-的溶液中:Ba2+、Na+、NO3-、Cl-
D.可与锌反应放出氢气的溶液中:Na+、Ca2+、Cl-、CO32-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在25℃、101 kPa条件下,C(s)、H2(g)、CH3COOH(l)的标准燃烧热分别为-393.5 kJ/mol、-285.8 kJ/mol、-870.3 kJ/mol,则1/2CH3COOH(l) ═ C(s)+H2(g)+1/2O2(g)的反应热为( )
A. +244.15 kJ/molB. +488.3 kJ/molC. -191 kJ/molD. +191 kJ/mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)工业上利用N2和H2合成NH3,NH3又可以进一步制备联氨(N2H4)等。由NH3制备N2H4的常用方法是NaClO氧化法,其离子反应方程式为___________,有学者探究用电解法制备的效率,装置如图,试写出其阳极电极反应式_________;

(2)乙醇汽油是被广泛使用的新型清洁燃料,工业生产乙醇(CH3CH2OH)的一种反应原理为:2CO(g)+4H2(g)![]() CH3CH2OH(g)+H2O(g) △H=-akJ/mol,己知:CO(g)+H2O(g)
CH3CH2OH(g)+H2O(g) △H=-akJ/mol,己知:CO(g)+H2O(g)![]() CO2(g)+H2(g) △H=-bkJ/mol,以CO2(g)与H2(g)为原料也可合成气态乙醇,并放出热量,写出该反应的热化学反应方程式:_________________。
CO2(g)+H2(g) △H=-bkJ/mol,以CO2(g)与H2(g)为原料也可合成气态乙醇,并放出热量,写出该反应的热化学反应方程式:_________________。
(3)如下图所示,某研究性学习小组利用上述燃烧原理设计一个肼(N2H4)─空气燃料电池(如图甲)并探究某些工业原理,其中乙装置中X为阳离子交换膜(即只允许阳离子通过)。
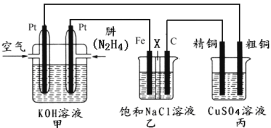
根据要求回答相关问题:
①甲装置中正极的电极反应式为:________________。
②乙装置中石墨电极产生产物如何检验______,电解一段时间后,乙池中的溶液呈___性。
③图中用丙装置模拟工业中的________原理,如果电解后丙装置精铜质量增加3.2g,则理论上甲装置中肼消耗质量为_____g。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知Cr(OH)3是类似Al(OH)3的两性氢氧化物,Ksp[Al(OH)3]=1.3×10-33,Ksp[Cr(OH)3]=6.3×10-31。如图为Cr和Al两种元素在水溶液中存在的形式与pH的关系,图中纵轴表示lgc(M3+)或lgc[M(OH)4-](其中M=Al或Cr)。下列说法错误的是( )

A.曲线N表示Al3+的浓度变化
B.在Al(OH)3和Cr(OH)3混合悬浊液中滴加NaOH溶液,Al(OH)3先溶解
C.在Al(OH)3和Cr(OH)3共沉淀的体系中![]() ≈4.8×102
≈4.8×102
D.若溶液中Al3+和Cr3+起始浓度均为0.1molL-1,通过调节pH能实现两种元素的分离
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)除去NaCO3粉末中混入的NaHCO3杂质用__________方法,化学方程式为____。
(2)除去氧化铜粉末中混入的氧化铝粉末通常用________试剂,离子方程式为________。
(3)通常用________试剂除去CO2中的HCl气体,离子方程式为________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com