
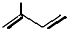
 :2-甲基-1,3-丁二烯;该物质与溴单质以物质的量之比1:1发生加成反应可能的产物有3 种;
:2-甲基-1,3-丁二烯;该物质与溴单质以物质的量之比1:1发生加成反应可能的产物有3 种;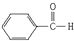 :苯甲醛;
:苯甲醛;分析 (1)选包含2个双键的最长碳链为主链;2-甲基-1,3-丁二烯与溴发生加成反应,可能是1,2加成、可能是3,4加成,也可能是1,3加成;
(2)该物质含有醛基,属于醛类;
(3)根据卤代烃的消去反应原理写出1-溴丙烷与氢氧化钠乙醇溶液共热的化学反应方程式
解答 解:选包含2个双键的最长碳链为主链,名称为2-甲基-1,3-丁二烯;2-甲基-1,3-丁二烯与溴发生加成反应,可能是1,2加成、可能是3,4加成,也可能是1,3加成,所以其加成产物有3种,故答案为:2-甲基-1,3-丁二烯;3;
(2)该物质含有醛基,属于醛类,名称为:苯甲醛,故答案为:苯甲醛;
(3)卤代烃在氢氧化钠醇溶液加热条件下发生消去反应,2-溴丙烷与氢氧化钠乙醇溶液加热反应方程式:CH2BrCH2CH3+NaOH$→_{△}^{醇}$CH2=CHCH3↑+H2O+NaBr,故答案为:CH2BrCH2CH3+NaOH$→_{△}^{醇}$CH2=CHCH3↑+H2O+NaBr;消去反应.
点评 本题考查了有机物的命名、有机反应方程式的书写等知识,题目难度中等,注意掌握常见有机物的命名原则,能够正确书写常见的有机反应方程式.


 黄冈天天练口算题卡系列答案
黄冈天天练口算题卡系列答案科目:高中化学 来源: 题型:选择题

| A. | 一段时间后铜片增重,盐桥中K+移向CuSO4溶液 | |
| B. | 正极反应为:Zn-2e-═Zn2+ | |
| C. | 电子从铜片经导线流向锌片 | |
| D. | 电池工作时Zn2+和Cu2+ 的浓度保持不变 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
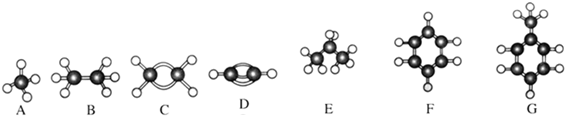
| 试剂 | |
| 乙烷混有少量乙烯 | |
| 溴苯混有少量溴单质 |
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | SO2和CO2都是酸性氧化物,都能与NaOH溶液反应 | |
| B. | Na2O和Na2O2组成元素相同,与CO2反应产物也完全相同 | |
| C. | NO和NO2的密度都比空气大,都可以用向上排空气法收集 | |
| D. | SO2和氯水都能使品红溶液褪色,但二者的作用原理是不同的 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com