
【题目】工业上用某矿渣(含有Cu2O、Al2O3、Fe2O3、SiO2)提取铜的操作流程如下:

已知: Cu2O + 2H+ = Cu + Cu2+ + H2O
沉淀物 | Cu(OH)2 | Al(OH)3 | Fe(OH)3 | Fe(OH)2 |
开始沉淀pH | 5.4 | 4.0 | 1.1 | 5.8 |
沉淀完全pH | 6.7 | 5.2 | 3.2 | 8.8 |
(1)固体混合物A中的成分是 。
(2)反应Ⅰ完成后,铁元素的存在形式为 。(填离子符号)请写出生成该离子的离子方程式 。
(3)x、y对应的数值范围分别是 、 。
(4)电解法获取Cu时,阴极反应式为 ,阳极反应式为 。
(5)下列关于NaClO调pH的说法正确的是 。
a. 加入NaClO可使溶液的pH降低
b. NaClO能调节pH的主要原因是由于发生反应ClO-+ H+![]() HClO, ClO-消耗H+,从而达到调节pH的目的
HClO, ClO-消耗H+,从而达到调节pH的目的
c .NaClO能调节pH的主要原因是由于NaClO水解ClO-+ H2O![]() HClO+OH-,OH-消耗H+ ,从而达到调节pH的目的
HClO+OH-,OH-消耗H+ ,从而达到调节pH的目的
(6)用NaClO调pH,生成沉淀B的同时生成一种具有漂白作用的物质,该反应的离子方程式为_________________________ 。
【答案】(1)SiO2、Cu(2分) (2)Fe2+ (2分) 2Fe3+ + Cu = Cu2+ + 2Fe2+(2分)
(3)3.2≤pH<4.0 , 5.2≤pH<5.4(2分)
(4)Cu2+ +2e- = Cu , 2Cl-- 2e- = Cl2↑(2分)
(5) b (2分)
(6)5ClO-+ 2Fe2+ + 5H2O = 2Fe(OH)3 + Cl-+ 4HClO(2分)
(或 2Fe2+ +7ClO-+ 2H++ 5H2O = 2Fe(OH)3 + Cl-+ 6HClO)
【解析】
试题分析:(1)加入硫酸发生了反应:Cu2O+2H+=Cu+Cu2++H2O,故固体A的成分是二氧化硅和铜;
(2)由于发生了反应,2Fe3++Cu=Cu2++2Fe2+,溶液中铁元素的存在形式为:Fe2+;
(3)调节PH=x,目的是生成沉淀氢氧化铁,PH应该大于3.2,小于4.0;调节PH=y,生成沉淀氢氧化铝,PH需要大于5.2,小于5.4;
(4)电解法获取Cu时,阴极铜离子得到电子,反应为:Cu2++2e-=Cu;阳极发生氧化反应,2Cl--2e-=Cl2↑;
(5)a、加入NaClO可使溶液的pH会升高,因为次氯酸根消耗了溶液中的氢离子,故a错误;b、由于NaClO能调节pH的主要原因是由于发生反应ClO-+H+HClO,ClO-消耗H+,故b正确;c、次氯酸钠调节溶液的PH,不是水解,是次氯酸根结合溶液中的氢离子,氢离子浓度下降,PH升高,故c错误;故选b;
(6)用NaClO调pH,生成沉淀B的同时生成一种具有漂白作用的物质,该反应的离子方程式是:5ClO-+2Fe2++5H2O=2Fe(OH)3+Cl-+4HClO;


科目:高中化学 来源: 题型:
【题目】应对雾霾污染、改善空气质量需要从多方面入手。
I.研究发现,NOx是雾霾的主要成分之一,NOx主要来源于汽车尾气。
已知:N2(g)+O2(g)![]() 2NO(g) △H=+180.50kJ·mol-1
2NO(g) △H=+180.50kJ·mol-1
2CO(g)+O2(g)![]() 2CO2(g) △H=-566.00 kJ·mol-1
2CO2(g) △H=-566.00 kJ·mol-1
为了减轻大气污染,人们提出在汽车尾气排气管口采用催化剂将NO和CO转化成无污染气体参与大气循环,写出该反应的热化学方程式 。
II.开发利用清洁能源可减少污染,解决雾霾问题。甲醇是一种可再生的清洁能源,具有广阔的开发和应用前景,一定条件下用CO和H2合成CH3OH:CO(g)+2H2(g)![]() CH3OH(g),在2L密闭容器中充入物质的量之比为1:2的CO和H2,在催化剂作用下充分反应。平衡混合物中CH3OH的体积分数在不同压强下随温度的变化如下图所示。
CH3OH(g),在2L密闭容器中充入物质的量之比为1:2的CO和H2,在催化剂作用下充分反应。平衡混合物中CH3OH的体积分数在不同压强下随温度的变化如下图所示。

(1)该反应的反应热△H 0(填“>”或“<”),压强的相对大小与P1 P2(填“>”或“<”)。
(2)该反应化学平衡常数表达式为 。
(3)下列各项中,不能说明该反应已经达到平衡的是 。
A.容器内气体压强不再变化
B.v(CO):v(H2):v(CH3OH)=1:2:1
C.容器内的密度不再变化
D.容器内混合气体的平均相对分子质量不再变化
E.容器内各组分的质量分数不再变化
(4)某温度下,在保证H2浓度不变的情况下,增大容器的体积,平衡 (填字母)。
A.向正反应方向移动 B.向逆反应方向移动 C.不移动
作出此判断的依据是 。
III.依据燃烧反应原理,合成的甲醇可以设计如图所示的燃料电池装置。

(1)负极电极反应式为 。
(2)电池工作时,若电流强度为I,1个电子所带电量为q,NA为阿伏伽德罗常数的值,则该装置每分钟消耗甲醇的物质的量为 mol(假设化学能全部转化为电能)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连。请回答以下问题:
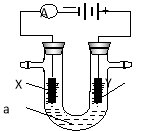
(1)若X、Y都是惰性电极,a是饱和NaCl溶液,实验开始时,同时在两边各滴入几滴酚酞试液,则
①电解池中X极上的电极反应式为 。
在X极附近观察到的实验现象是 。
②Y电极是电解池的 极,该电极上的电极反应式为 。
(2)如要用电解方法精炼粗铜,电解液a选用CuSO4溶液,则
①X电极的材料是 ,电极反应式为 。
②Y电极的材料是 ,电极反应式为 。
(说明:杂质发生的电极反应不必写出)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知A元素原子的L层比B元素原子的L层少3个电子,B元素原子核外电子数比A元素原子核外电子总数多5个,则A、B两元素形成的化合物可表示为
A. BA2 B. BA3 C. A3B2 D. B3A2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】把a、b、c、d四块金属片浸入稀硫酸中,用导线两两相连可以组成几个原电池。若a、b 相连时a为负极;c、d相连时电流由d到c;a、c相连时c极上产生大量气泡;b、d相连时b上有大量气泡产生,则四种金属的活动性顺序由强到弱为
A. a>b>c>d B. c>a>b>d C. a>c>d>b D. b>d>c>a
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】聚苯乙烯可用于制备高频绝缘材料,苯乙烯在一定条件下存在如下图转化关系。

请回答下列问题:
(1)由苯乙烯合成高聚物的化学方程式为 。
(2)写出F中官能团的名称:
(3)C可能的结构简式有 。
(4)H有多种同分异构体,请写出官能团不完全相同的两种同分异构体的结构简式:
。
(5)反应③的化学方程式是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】海洋植物如海带、海藻中含有丰富的碘元素,碘元素以碘离子的形式存在。实验室里从海藻中提取碘的流程如下:

⑴ 在提取碘的过程中有关实验的操作名称:① ,③ ;写出过程②中有关反应的化学方程式: 。
⑵提取碘的过程中,可供选择的有机试剂是 。
A.酒精 B.苯 C.乙酸 D.四氯化碳
⑶为使海藻灰中碘离子转化为碘的有机溶液,实验室里有烧杯、玻璃棒、集气瓶、酒精灯、导管、圆底烧瓶、石棉网以及必要的夹持仪器、物品,尚缺少的玻璃仪器是 。
⑷从含碘的有机溶液中提取碘和回收有机溶剂,还需经过蒸馏。指出如图所示实验装置中的错误之处: ; ; 。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,下列各组离子一定能在指定溶液中大量共存的是( )
A.使酚酞变红色的溶液中:Na+、Al3+、SO42﹣、Cl﹣
B.![]() =1×10﹣13molL﹣1的溶液中:NH4+、Ca2+、Cl﹣、NO3﹣
=1×10﹣13molL﹣1的溶液中:NH4+、Ca2+、Cl﹣、NO3﹣
C.与Al反应能放出H2的溶液中:Fe2+、K+、NO3﹣、SO42﹣
D.水电离的c(H+)=1×10﹣13molL﹣1的溶液中:K+、Na+、AlO2﹣、CO32﹣
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com