
设阿伏加德罗常数为NA,下列说法正确的是( )
A.2 L 0.5 mol·L-1硫酸钾溶液中阴离子所带电荷数为NA
B.常温常压下,14g氮气中含有 NA个原子
C.1mol/LNaCl溶液中含有NA个氯离子
D.等质量的丙烯和乙烯气体中氢原子的个数均为6NA
科目:高中化学 来源:2015届广东省广州市高三上学期期中考试理综化学试卷(解析版) 题型:选择题
类推是学习和研究的重要思维方法。下列类推结论正确的是
| 化学事实 | 类推结论 |
A | Al在O2中燃烧生成Al2O3 | Fe在O2中燃烧也生成Fe2O3 |
B | pH=3的盐酸稀释1000倍后pH=6 | pH=6的盐酸稀释1000倍后pH=9 |
C | 用电解熔融MgCl2的方法冶炼金属镁 | 用电解熔融NaCl的方法制取金属钠 |
D | 将SO2通入BaCl2溶液中无沉淀生成 | 将SO2通入Ba(NO3)2溶液中也无沉淀生成 |
查看答案和解析>>
科目:高中化学 来源:2015届广东省佛山市高三9月考化学试卷(解析版) 题型:选择题
下列离子方程式书写正确的是
A.将少量的H2S气体通入硫酸铜溶液中: H2S+Cu2+=CuS↓+2H+
B.将NO2气体通入水中:2NO2+H2O= NO3-+ NO↑+2H+
C.ICl 和Cl2的化学性质相似,将ICl通入KOH溶液中:ICl+2OH-= I-+ ClO-+H2O
D.往100ml 1.5mol/L的FeBr2 溶液中通入0.15mol Cl2:2Br-+Cl2=Br2+2Cl-
查看答案和解析>>
科目:高中化学 来源:2015届广东省中山市高三上学期第二次模拟考试化学试卷(解析版) 题型:实验题
(12分)二氧化铈CeO2是一种重要的稀土氧化物。平板电视显示屏生产过程中产生大量的废玻璃粉末(含SiO2、Fe2O3、CeO2以及其他少量可溶于稀酸的物质)。某课题组以此粉末为原料回收铈,设计实验流程如下:
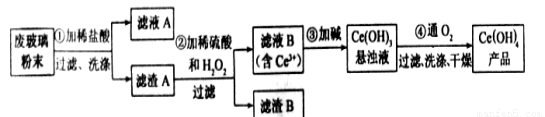
(1)洗涤滤渣A的目的是为了去除 (填离子符号),检验滤渣A是否洗涤干净的方法是 。
(2)第②步反应的离子方程式是 ,滤渣B的主要成分是 。
(3)萃取是分离稀土元素的常用方法,已知化合物TBP作为萃取剂能将铈离子从水溶液中萃取出来,TBP (填“能”或“不能”)与水互溶。实验室进行萃取操作是用到的主要玻璃仪器有 、烧杯、量筒等。
(4)取上述流程中得到的Ce(OH)4[M=208g/mol]产品0.500g,加硫酸溶解后,用0.1000mol?L-1FeSO4标准溶液滴定(铈被还原为Ce3+),消耗20.00mL标准溶液,该产品中Ce(OH)4的质量分数为 。(保留两位小数)
查看答案和解析>>
科目:高中化学 来源:2015届广东省中山市高三上学期第二次模拟考试化学试卷(解析版) 题型:选择题
下述实验设计能够达到目的的是( )
选项 | 实验目的 | 实验设计 |
A | 证明SO2有漂白性 | 把SO2通入品红溶液中 |
B | 除去Cu粉中的CuO | 向混合物中滴加适量稀硝酸 |
C | 检验溶液中是否含有Fe2+ | 向溶液中滴入KSCN溶液,再滴加氯水 |
D | 证明H2CO3酸性比H2SiO3强 | Na2CO3和SiO2在高温下熔融反应 |
查看答案和解析>>
科目:高中化学 来源:2015届广东省中山市高三上学期第二次模拟考试化学试卷(解析版) 题型:选择题
下列说法正确的是
A.S在纯氧中燃烧可生成SO3
B.用澄清石灰水可鉴别CO2和SO2
C.SO2能使KMnO4溶液褪色
D.CO2通入CaCl2溶液中能产生白色沉淀
查看答案和解析>>
科目:高中化学 来源:2015届广东省中山市等五校联考高三第一学期化学试卷(解析版) 题型:选择题
用下列实验装置进行的实验中,说法正确的是( )
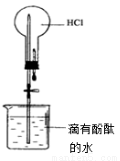
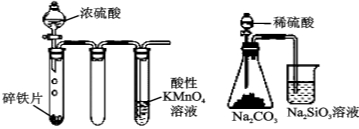

实验① 实验② 实验③ 实验④
A.实验①:打开止水夹,烧瓶内出现红色喷泉
B.实验②:铁片最终完全溶解,且高锰酸钾溶液褪色
C.实验③:所示实验可比较硫、碳、硅三种元素的非金属性强弱
D.实验④:烧杯中液体变为红褐色后,继续加热煮沸,会出现浑浊
查看答案和解析>>
科目:高中化学 来源:2015届广东省东莞市高三第一次调研考试理科化学试卷(解析版) 题型:填空题
(16分)某新型液晶有机物基元IV的合成线路如下:
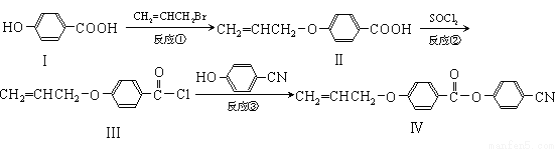
(1)Ⅰ的分子式 ,Ⅰ中含氧官能团的名称 ,反应①的类型为 反应。
(2)CH2=CHCH2Br与NaOH水溶液反应的化学方程式 (注明条件)。
(3)II可发生加聚反应,所得产物的结构简式 。
(4)有关化合物Ⅰ和II的说法中,不正确的是 。
A.1molⅠ充分燃烧需要消耗6mol O2 B.1molⅠ最多可消耗2mol NaOH
C.II能使溴的CCl4溶液褪色 D.II能使酸性KMnO4溶液褪色
(5)一定条件下, 也可与III发生类似反应③的反应,生成有机物V,V的结构简式是 。
也可与III发生类似反应③的反应,生成有机物V,V的结构简式是 。
(6)化合物I的同分异构体中,苯环上一溴代产物只有两种,遇FeCl3溶液显紫色,还能发生银镜反应的化合物有多种,写出其中一种同分异构体的结构简式 。
查看答案和解析>>
科目:高中化学 来源:2015届山东省高三上学期第二次月考联考化学试卷(解析版) 题型:实验题
(10分)下图所示是用于气体制备、干燥(或除杂质)、性质验证、尾气处理的部分仪器装置(加热及夹持固定装置均已略去,各装置可重复使用也可不用)。请根据下列要求回答问题。
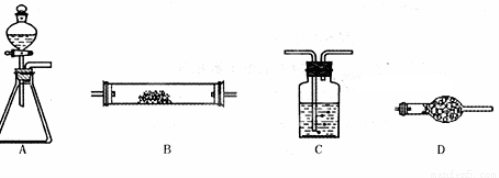
(1)若用A-C-D-B组合进行氢气还原氧化铜实验。分液漏斗中的试剂是盐酸,C中试剂是水,其作用是 ;A中反应开始一段时间后,再加热B。加热B之前的实验操作是 。
(2)为验证氯气不能使干燥的红布条褪色,置红布条于B中,按A-C-B-D连接成实验装置体系。A锥形瓶中试剂选用高锰酸钾晶体,则分液漏斗中的液体是 (填名称);C中试剂是 (填名称)。已知高锰酸钾反应生成+2价的锰离子,写出此法制备氯气的离子方程式 。
(3)为了进行氨的催化氧化实验,若锥形瓶中盛装足量的Na2O2粉末,分液漏斗中盛装浓氨水,慢慢打开分液漏斗的活塞,产生的气体通过红热的铂粉,各仪器装置按气流方向从左到右连接顺序是 ;(填字母)装置B中发生反应的化学方程式为 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com