
【题目】将一定量的钠、铝合金置于水中,合金全部溶解,得到20mL、pH=14的溶液。然后用1mol/L的盐酸滴定至沉淀量最大时,消耗盐酸40mL。原合金中钠的质量为( )
A. 0.92g B. 0.69g C. 0.64g D. 0.23g
【答案】A
【解析】Na、Al合金置于水中发生的反应有2Na+2H2O=2NaOH+H2↑、2Al+2NaOH+2H2O=2NaAlO2+3H2↑,由于得到的溶液pH=14,溶液中溶质为NaAlO2和NaOH;向溶液中加入盐酸至沉淀量最大时,发生的反应有NaOH+HCl=NaCl+H2O、NaAlO2+HCl+H2O=Al(OH)3↓+NaCl,此时溶液中溶质为NaCl,根据电荷守恒和原子守恒计算。
Na、Al合金置于水中发生的反应有2Na+2H2O=2NaOH+H2↑、2Al+2NaOH+2H2O=2NaAlO2+3H2↑,由于得到的溶液pH=14,溶液中溶质为NaAlO2和NaOH;向溶液中加入盐酸至沉淀量最大时,发生的反应有NaOH+HCl=NaCl+H2O、NaAlO2+HCl+H2O=Al(OH)3↓+NaCl,此时溶液中溶质为NaCl,根据电荷守恒和原子守恒,n(Na)=n(Na+)=n(Cl-)=n(HCl)=1mol/L![]() 0.04L=0.04mol,原合金中Na的质量为0.04mol
0.04L=0.04mol,原合金中Na的质量为0.04mol![]() 23g/mol=0.92g,答案选A。
23g/mol=0.92g,答案选A。


 波波熊暑假作业江西人民出版社系列答案
波波熊暑假作业江西人民出版社系列答案 学而优暑期衔接南京大学出版社系列答案
学而优暑期衔接南京大学出版社系列答案 Happy holiday欢乐假期暑假作业广东人民出版社系列答案
Happy holiday欢乐假期暑假作业广东人民出版社系列答案科目:高中化学 来源: 题型:
【题目】能正确表达下列反应的离子方程式为
A. NaHCO3溶液中加足量Ba(OH)2溶液:2HCO3-+Ba2++2OH-![]() BaCO3↓+CO32-+2H2O
BaCO3↓+CO32-+2H2O
B. 少量SO2通入Ca(ClO)2溶液中:SO2+H2O+Ca2++2ClO—![]() CaSO3↓+2HClO
CaSO3↓+2HClO
C. 用高锰酸钾标准溶液滴定草酸:2MnO4-+16H++5C2O42-![]() 2Mn2++10CO2↑+8H2O
2Mn2++10CO2↑+8H2O
D. 电解饱和食盐水获取烧碱和氯气: 2Cl—+ 2H2O![]() H2↑+ Cl2↑+2OH—
H2↑+ Cl2↑+2OH—
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】聚合物H ( )是一种聚酰胺纤维,广泛用于各种刹车片,其合成路线如下:
)是一种聚酰胺纤维,广泛用于各种刹车片,其合成路线如下:

已知:①C、D、G均为芳香族化合物,分子中均只含两种不同化学环境的氢原子。
②Diels-Alder反应:![]() 。
。
(1)生成A的反应类型是_______。D的名称是_______。F中所含官能团的名称是_______。
(2)B的结构简式是_______;“B→C”的反应中,除C外,另外一种产物是_______。
(3)D+G→H的化学方程式是______。
(4)Q是D的同系物,相对分子质量比D大14,则Q可能的结构有______种,其中核磁共振氢谱有4组峰,且峰面积比为1:2:2:3的结构简式为______(任写一种)。
(5)已知:乙炔与1,3-丁二烯也能发生Diels-Alder反应。请以1,3-丁二烯和乙炔为原料,选用必要的无机试剂合成 ,写出合成路线__________(用结构简式表示有机物,用箭头表示转化关系,箭头上注明试剂和反应条件)。
,写出合成路线__________(用结构简式表示有机物,用箭头表示转化关系,箭头上注明试剂和反应条件)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在密闭容器中进行反应:2SO2(g)+O2(g)![]() 2SO3(g)(正反应放热),如图是某次实验的化学反应速率随时间变化的图像,推断在t1时刻突然变化的条件可能是( )
2SO3(g)(正反应放热),如图是某次实验的化学反应速率随时间变化的图像,推断在t1时刻突然变化的条件可能是( )

A. 催化剂失效 B. 减小生成物的浓度
C. 降低体系温度 D. 增大容器的体积
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】W、X、Y、Z四种短周期元素在周期表中的相对位置如图所示。W、X、Y、Z原子的最外层电子数之和为21。下列说法中错误的是( )
![]()
A. 元素X的单质能与强酸、强碱反应B. 元素W、X与钠元素可形成化合物Na3XW6
C. 气态氢化物的稳定性:W>YD. 简单阴离子的还原性:W>Z
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】K2Cr2O7溶液中存在平衡:Cr2O72-(橙色)+H2O![]() 2CrO42-(黄色)+2H+。用K2Cr2O7溶液进行下列实验:
2CrO42-(黄色)+2H+。用K2Cr2O7溶液进行下列实验:

结合实验,下列说法正确的是
A. ①中溶液变黄,③中溶液橙色加深
B. ②中Cr2O72-被C2H5OH氧化
C. K2Cr2O7在碱性条件下的氧化性比酸性条件更强
D. 若向④中加入70%H2SO4溶液至过量,溶液变为绿色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,用0.01000 mol·L-1的盐酸滴定0.01000 mol·L-1NaA溶液20.00mL。滴定曲线如图所示,下列说法正确的是
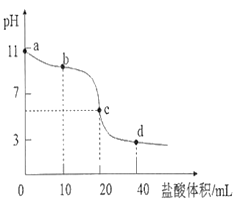
A. a点到d点的过程中,等式c(HA)+c(A—)=0.01000 mol·L—1恒成立
B. b点时,溶液中微粒浓度大小关系为:c(A—)>c(Cl —)>c(HA)>c(OH—)>c(H+)
C. c点时,溶液中微粒浓度存在关系:c(Na+)+c(H+) = c(HA)+c(OH—)+2c(A—)
D. d点时,溶液中微粒浓度存在关系:c(OH—)+c(A—)=c(H+)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com