
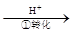 Cr2O72��
Cr2O72��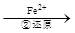 Cr3+
Cr3+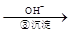 Cr(OH)3��
Cr(OH)3��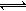 Cr2O72��(��ɫ)+H2O
Cr2O72��(��ɫ)+H2O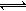 Cr3+(aq)+3OH�D(aq)
Cr3+(aq)+3OH�D(aq)

 ��ĩ�����ϵ�д�
��ĩ�����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
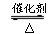 2SO3 ���Ը÷�Ӧ���й�˵���������
2SO3 ���Ը÷�Ӧ���й�˵���������| A���÷�Ӧ�ǿ��淴Ӧ | B����Ӧ��SO2��ȫ��ת��ΪSO3 |
| C�������ܼӿ�÷�Ӧ������ | D�������¶��ܼӿ�÷�Ӧ������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
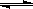 2SO3 �ﵽƽ���ͨ��
2SO3 �ﵽƽ���ͨ��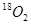 һ��ʱ���
һ��ʱ���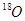 �����ڣ� ��
�����ڣ� ��| A��SO3��O2 | B��SO2��SO3 | C��SO2��O2 | D��SO2��SO3��O2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
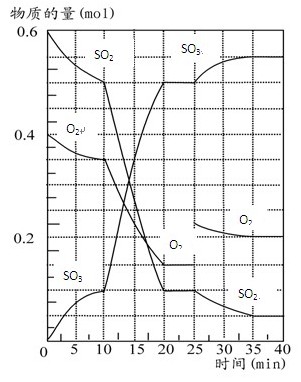
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
| A��HCl��� | B��H2SO4��� |
| C��CH3COOH��� | D��һ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
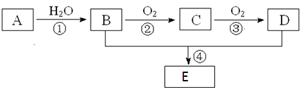
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ�������
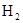 ��443K��473K�¶�������������������̼ԭ����Ϊ5��8����������390�棬300������ѹ�£�����ˮú��Ϊԭ�ϣ����Ժϳɼ״���
��443K��473K�¶�������������������̼ԭ����Ϊ5��8����������390�棬300������ѹ�£�����ˮú��Ϊԭ�ϣ����Ժϳɼ״���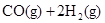

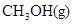 ����CO��
����CO��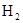 �ı�����ͬʱ����CO��ת����ƽ�������м״��ĺ�������Ӱ�죮��m��ʾ
�ı�����ͬʱ����CO��ת����ƽ�������м״��ĺ�������Ӱ�죮��m��ʾ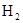 ��CO���ʵ���֮�ȣ�aΪCO��ת���ʣ�yΪƽ��������
��CO���ʵ���֮�ȣ�aΪCO��ת���ʣ�yΪƽ�������� ��������������Ƶ���m��a��y֮��Ĺ�ϵʽ��
��������������Ƶ���m��a��y֮��Ĺ�ϵʽ���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
 2HI��g������H<0�����ﵽƽ�⡣HI���������w��HI����ʱ��仯�����ߣ�����ʾ��
2HI��g������H<0�����ﵽƽ�⡣HI���������w��HI����ʱ��仯�����ߣ�����ʾ��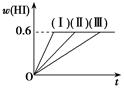
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 CO2(g)+H2(g)�ﵽƽ�����֪�÷�Ӧƽ�ⳣ��ΪK=1.0���ﵽ�µ�ƽ���CO2��H2�����ʵ���֮��Ϊ�� ��
CO2(g)+H2(g)�ﵽƽ�����֪�÷�Ӧƽ�ⳣ��ΪK=1.0���ﵽ�µ�ƽ���CO2��H2�����ʵ���֮��Ϊ�� ��| A��1.2mol | B��1.5mol | C��1.8mol | D��2.5mol |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com