
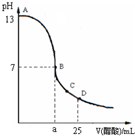
 25℃时,在25mL 0.1mol/L的NaOH溶液中,逐滴加入0.2mol/L的CH3COOH溶液,溶液的pH变化如图所示,下列分析的结论中不正确的是( )
25℃时,在25mL 0.1mol/L的NaOH溶液中,逐滴加入0.2mol/L的CH3COOH溶液,溶液的pH变化如图所示,下列分析的结论中不正确的是( )| A、B点的横坐标a=12.5 |
| B、C点时溶液中有:c(CH3COO-)>c(Na+)>c(H+)>c(OH-) |
| C、D点时溶液中有:c(CH3COO-)+c(CH3COOH)=2 c(Na+) |
| D、曲线上A、B间的任意一点,溶液中都有:c(Na+)>c(CH3COO-)>c(OH-)>c(H+) |


科目:高中化学 来源: 题型:
| A、Na+、H+、NO3-、CO32- |
| B、Na+、Fe3+、Cl-、SO42- |
| C、K+、Cu2+、SO42-、OH- |
| D、Na+、Al3+、NO3-、Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:
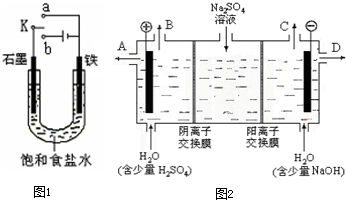
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、铜片跟稀硝酸反应:Cu+4H++NO3-═Cu2++NO↑+2H2O |
| B、AlCl3溶液中加入过量氨水:Al3++4OH-═AlO2-+2H2O |
| C、FeBr2溶液与等物质的量Cl2反应:2Fe2++2Br-+2Cl2═2Fe3++4Cl-+Br2 |
| D、向小苏打溶液中加入过量的石灰水:Ca2++2OH-+2HCO3-═CaCO3↓+CO32-+2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、NaHS水解反应:HS-+H2O?H3O++S2- | ||
| B、明矾加入在水中起净化作用的原因:Al3++3H2O?Al(OH)3(胶体)+3H+ | ||
C、氢氧化钡溶液与稀硫酸反应:Ba2++SO
| ||
| D、碳酸氢钠溶液中加入过量Ba(OH)2溶液:2HCO3-+Ba2++2OH-=BaCO3↓+CO32-+2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、达到化学平衡时,4v正(O2)=5v逆(NO) |
| B、若单位时间内生成x mol NO,同时消耗x mol NH3,则反应达到平衡状态 |
| C、达到化学平衡时,若缩小容器体积,则正反应速率减少,逆反应速率增大 |
| D、在恒容容器中,若混合气体密度不再改变,则反应达到平衡状态 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、氢氧化钡与稀硫酸反应:Ba2++SO42-=BaSO4↓ |
| B、Al2O3溶于盐酸中:O2-+2H+=H2O |
| C、氯化铝溶液中加入少量氨水:Al3++3OH-=Al(OH)3↓ |
| D、氯气与水反应 Cl2+H2O?H++Cl-+HClO |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、强碱性溶液中:K+、Al3+、Cl-、SO42- |
| B、pH=0的溶液中:Na+、Fe3+、NO3-、SO42- |
| C、含有1mol?L-1Fe3+的溶液中:K+、Mg2+、I-、NO3 |
| D、由水电离的c(H+)=1×10-14的溶液中:K+、Ca2+、Cl-、HCO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com