
| A. | NaOH | B. | AgNO3 | C. | BaCl2 | D. | Ba(OH)2 |
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
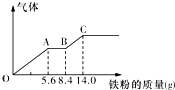 某稀硫酸和稀硝酸的混合溶液200mL,平均分成两份.向其中一份中逐渐加入铜粉,最多能溶解9.6g.向另一份中逐渐加入铁粉,产生气体的量随铁粉质量增加的变化如图所示(已知硝酸只被还原为NO气体).下列分析或结果错误的是( )
某稀硫酸和稀硝酸的混合溶液200mL,平均分成两份.向其中一份中逐渐加入铜粉,最多能溶解9.6g.向另一份中逐渐加入铁粉,产生气体的量随铁粉质量增加的变化如图所示(已知硝酸只被还原为NO气体).下列分析或结果错误的是( )| A. | H2SO4浓度为2.5 mol•L-1 | |
| B. | OA段产生的是NO,AB段的反应为Fe+2Fe3+═3Fe2+,BC段产生氢气 | |
| C. | 第二份溶液中最终溶质为FeSO4 | |
| D. | 原混合酸中NO3-物质的量为0.1 mol |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在高温下,有1 mol Fe与足量的水蒸气反应,转移电子的数目为3NA | |
| B. | 1 mol的羟基与1 mol的氢氧根离子所含电子数均为10NA | |
| C. | 酸性溶液中可能大量存在Na+、ClO?、SO42?、I? | |
| D. | $\frac{c({H}^{+})}{c(O{H}^{-})}$=1012的溶液中:NH4+、Al3+、NO3-、Cl-离子组能够大量共存 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
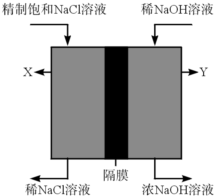 以海水为主要原料的海洋化学工业,被称为“蓝色化工”.氯碱工业是“蓝色化工”重要的组成部分,其化学反应原理是电解饱和食盐水.
以海水为主要原料的海洋化学工业,被称为“蓝色化工”.氯碱工业是“蓝色化工”重要的组成部分,其化学反应原理是电解饱和食盐水.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氢氧化钠 | B. | 过氧化氢 | C. | 次氯酸钙 | D. | 硫酸亚铁 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | X与Y形成化合物时,X显负价,Y显正价 | |
| B. | X的第一电离能一定大于Y | |
| C. | 最高价含氧酸的酸性:X对应的酸性强于Y对应的酸性 | |
| D. | 气态氢化物的稳定性:HnY小于HmX |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com