
 CO2(g)+H2(g) △H>0。在850℃时,K=1。?此温度下,若向一容积可变的密闭容器中同时充入1.0 mol CO,3.0 mol H2O,
CO2(g)+H2(g) △H>0。在850℃时,K=1。?此温度下,若向一容积可变的密闭容器中同时充入1.0 mol CO,3.0 mol H2O, 探究与巩固河南科学技术出版社系列答案
探究与巩固河南科学技术出版社系列答案科目:高中化学 来源:不详 题型:单选题
 CuSO4·xH2O,当向硫酸铜溶液中加少量无水硫酸铜粉末后,下列说法中正确的是
CuSO4·xH2O,当向硫酸铜溶液中加少量无水硫酸铜粉末后,下列说法中正确的是| A.溶液中Cu2+浓度增大 | B.溶液中Cu2+数目减少 |
| C.该硫酸铜晶体体积增大 | D.溶液的蓝色变浅 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
| 实验步骤 | 向3—4 mL 1 mol/L的CaCl2溶液中滴入1mol/L的Na2SO4溶液至反应完全。 |
| 实验现象 | 产生白色沉淀 |
| 离子方程式 | (1) |
| 小组讨论交流 | 向上述反应后的清液中滴入适量1mol/L的Na2CO3溶液会出现什么现象 |
| 假设出现的实验现象,说明理由 | 假设Ⅰ: 无现象; 理由:反应没有限度,Ca2+沉淀完全 假设Ⅱ:(2) ,理由:(3) |
| 证明你的假设 | 现象:产生大量的白色沉淀 |
| 离子方程式 | (4) |
| 实验结论 | (5) |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
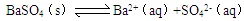 的下列说法正确的是( )
的下列说法正确的是( )| A.溶液的温度升高,BaSO4的溶度积常数不变 |
| B.在Na2SO4溶液中,BaSO4的溶解度不变 |
| C.在BaCl2溶液中,BaSO4的溶度积常数变小 |
| D.精制NaCl时,在溶液中加入稍过量的BaCl2溶液是为了更好地除去SO42-等离子 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.40 mL 1 mol/L的BaCl2溶液 |
| B.30 mL 2 mol/L的Ba(OH)2溶液 |
| C.10 mL纯水 |
| D.50 mL 0.1 mol/L的H2SO4溶液 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.25 ℃时,饱和Mg(OH)2溶液与饱和MgF2溶液相比,前者的C(Mg2+)大 |
| B.25 ℃时,在Mg(OH)2的悬浊液中加入少量的NH4Cl固体,C(Mg2+)增大 |
| C.25 ℃时,Mg(OH)2固体在20 mL 0.01 molL-1氨水中的Ksp比在20 mL 0.01molL-1NH4Cl溶液中的Ksp小 |
| D.25 ℃时,在Mg(OH)2悬浊液中加入NaF溶液后,Mg(OH)2不可能转化为MgF2 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题

查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

 Cr2O72—(橙色)+H2O
Cr2O72—(橙色)+H2O Cr3+(aq)+3OH—(aq)
Cr3+(aq)+3OH—(aq)查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
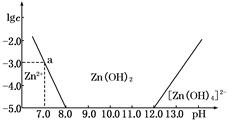
| c(HCl) | | | | | | | |
| (mol/L) | 0.50 | 1.00 | 2.04 | 2.90 | 4.02 | 5.16 | 5.78 |
| 103c(PbCl2) | | | | | | | |
| (mol/L) | 5.10 | 4.91 | 5.21 | 5.90 | 7.48 | 10.81 | 14.01 |
| A.随着盐酸浓度的增大,PbCl2固体的溶解度先变小后又变大 |
| B.PbCl2固体在0.50 mol/L盐酸中的溶解度小于在纯水中的溶解度 |
| C.PbCl2能与浓盐酸反应生成一种难电离的阴离子(络合离子) |
| D.PbCl2固体可溶于饱和食盐水 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com