
由硫酸钾、硫酸铝和硫酸组成的混合溶液,其中c(H+)=0.1mol/L,c(Al3+)=0.4mol/L,c(SO42﹣)=0.8mol/L,则c(K+)为()
A. 0.15 mol/L B. 0.2 mol/L C. 0.3 mol/L D. 0.4 mol/L
考点: 物质的量浓度的相关计算;电解质在水溶液中的电离.
专题: 守恒法.
分析: 溶液中存在3c(Al3+)+c(K+)+c(H+)=2c(SO42﹣)+c(OH﹣),根据溶液电荷守恒计算.
解答: 解:根据溶液电荷守恒,溶液中存在3c(Al3+)+c(K+)+c(H+)=2c(SO42﹣)+c(OH﹣),而溶液中c(OH﹣)很小,可以忽略不计,
则有3c(Al3+)+c(K+)+c(H+)=2c(SO42﹣),所以:c(K+)=2c(SO42﹣)﹣3c(Al3+)﹣c(H+),
c(K+)═2×0.8mol/L﹣3×0.4mol/L﹣0.1mol/L=0.3mol/L;
故选C.
点评: 本题考查溶液物质的量浓度的计算,题目难度不大,可利用电荷守恒计算.


 口算心算速算应用题系列答案
口算心算速算应用题系列答案 同步拓展阅读系列答案
同步拓展阅读系列答案科目:高中化学 来源: 题型:
如图是部分短周期元素化合价与原子序数的关系图,下列说法正确的是()
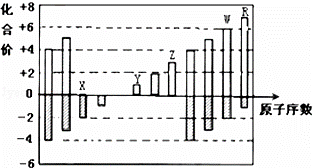
A. 原子半径:Z>Y>X
B. 气态氢化物的稳定性:R<W
C. WX3和水反应形成的化合物是离子化合物
D. Y和Z两者最高价氧化物对应的水化物能相互反应
查看答案和解析>>
科目:高中化学 来源: 题型:
人们常将在同一原子轨道上运动的,自旋方向相反的2个电子,称为“电子对”;将在同一原子轨道上运动的单个电子,称为“未成对电子”.以下有关主族元素原子的“未成对电子”的说法,错误的是( )
|
| A. | 核外电子数为奇数的基态原子,其原子轨道中一定含有“未成对电子” |
|
| B. | 核外电子数为偶数的基态原子,其原子轨道中一定不含“未成对电子” |
|
| C. | 核外电子数为偶数的基态原子,其原子轨道中可能含有“未成对电子” |
|
| D. | 核外电子数为奇数的基态原子,其原子轨道中可能不含“未成对电子” |
查看答案和解析>>
科目:高中化学 来源: 题型:
下表是元素周期表的一部分,表中所列的字母分别代表一种化学元素.
| a |
| ||||||||||||||||
| b | c | d | e | f |
| ||||||||||||
| g | h | i | j | k | l | m |
| ||||||||||
| n | o |
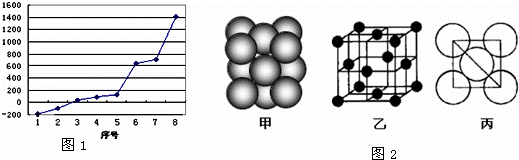
试回答下列问题:
(1)请写出字母O代表的元素符号 ,该元素在周期表中的位置 .
(2)第三周期8种元素按单质熔点高低的顺序如右图,其中序号“8”代表 (填元素符号);其中电负性最大的是 (填如图1中的序号).
(3)由j原子跟c原子以1:1相互交替结合而形成的晶体,晶型与晶体j相同.两者相比熔点更高的是 (填化学式),试从结构角度加以解释: .
(4)k与l形成的化合物kl2的电子式是 ,它在常温下呈液态,形成晶体时,属于 晶体.
(5)i单质晶体中原子的堆积方式如图2(甲)所示,其晶胞特征如图2(乙)所示,原子之间相互位置关系的平面图如图2(丙)所示.若已知i的原子半径为d,NA代表阿伏加德罗常数,i的相对原子质量为M,请回答:
一个晶胞中i原子的数目为 ,该晶体的密度_ (用M、NA、d表示).
(6)a与d构成的阳离子和i的阳离子可与硫酸根形成一种复盐,向该盐的浓溶液中逐滴加入浓氢氧化钡溶液,产生的现象有:①溶液中出现白色沉淀并伴有有刺激性气味气体放出,②沉淀逐渐增多后又逐渐减少直至最终沉淀的量不变.写出沉淀的量不变时发生反应的离子方程式 .
查看答案和解析>>
科目:高中化学 来源: 题型:
下列离子方程式正确的是()
A. 澄清的石灰水与稀盐酸反应Ca(OH)2+2H+═Ca2++2H2O
B. 钠与水的反应Na+2H2O═Na++2OH﹣+H2↑
C. 硫酸氢钠溶液与少量氢氧化钡溶液混合:2H++SO42﹣+Ba2++2OH﹣═BaSO4↓+2H2O
D. 向沸水中滴加FeCl3溶液制备Fe(OH)3胶体:Fe3++3H2O Fe(OH)3↓+3H+
Fe(OH)3↓+3H+
查看答案和解析>>
科目:高中化学 来源: 题型:
下列物质与常用危险化学品的类别不对应的是()
A. CH4、汽油﹣易燃液体 B. H2SO4、NaOH﹣腐蚀品
C. K、Na﹣遇湿易燃物品 D. KMnO4、K2Cr2O2﹣氧化剂
查看答案和解析>>
科目:高中化学 来源: 题型:
下列结果是马虎同学回答同桌提问的答案,你认为需要改正的是()
①微粒半径:S2﹣>Cl﹣>S>Cl ②氢化物稳定性:HF>HCl>H2S>PH3③还原性:Na>Mg>Al>K ④氧化性:Cl2>S>O2>F2 ⑤酸性:H2SO4>HClO4>H2SiO3>H3PO4 ⑥得电子能力:F>Cl>Br>I.
A. 只有③ B. ③④⑤ C. ②④⑤⑥ D. ③④⑤⑥
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com