
| A. | 氧元素的主要化合价为-2、+6 | B. | N2H4是共价化合物 | ||
| C. | 氮的最高价态氧化物为NO2 | D. | 原子半径:H<N<O |
 名师指导期末冲刺卷系列答案
名师指导期末冲刺卷系列答案 开心蛙口算题卡系列答案
开心蛙口算题卡系列答案科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②③④ | B. | ①②④⑥ | C. | ①②③④⑥ | D. | ①②③④⑤⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
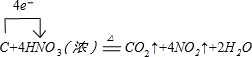 ;
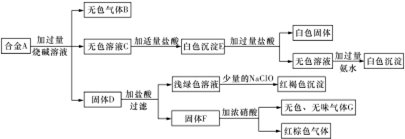
;
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
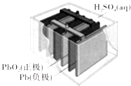
| A. | 铅蓄电池属于二次电池 | |
| B. | 实际使用过程中可以无限次充放电 | |
| C. | 使用过程中负极发生氧化反应 | |
| D. | 铅蓄电池体积大有污染还不是最理想的电池 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用M表示此反应的反应速率γ(M)=0.1a mol•(L•min)-1 | |
| B. | 当混合气体的质量不再发生变化时,说明反应达到平衡状态 | |
| C. | 向平衡后的体系中加入l mol M,平衡向逆反应方向移动 | |
| D. | 向上述平衡体系中再充入l mol X,平衡正向移动,因为此时γ正增大,γ逆减小 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com