
【题目】已知常温下Ksp(AgCl)=1.6×10﹣10、Ksp(AgI)=2.0×10﹣16 , 下列说法中正确的是( )
A.含有大量Cl﹣的溶液中肯定不存在Ag+
B.AgI悬浊液中加入少量KI粉末,平衡AgI(s)?Ag+(aq)+I﹣(aq)向左移动,溶液中离子的总浓度会减小
C.AgCl悬浊液中逐渐加入KI固体至c(I﹣)= ![]() mol?L﹣1时,AgCl开始向AgI沉淀转化
mol?L﹣1时,AgCl开始向AgI沉淀转化
D.向浓度均为0.01 mol?L﹣1的KCl和KI的混合溶液中滴加AgNO3溶液,当Cl﹣开始沉淀时,溶液中I﹣的浓度为1.25×10﹣8 mol?L﹣1
【答案】D
【解析】解:A.一般认为离子浓度为10﹣5molL﹣1时沉淀完全,则含有大量Cl﹣的溶液中,肯定存在少量的Ag+ , 故A错误; B.加入少量KI粉末,平衡AgI(s)Ag+(aq)+I﹣(aq)向左移动,c(I﹣)浓度增大,c(Ag+)减小,但引入K+ , 则离子的总浓度会增大,故B错误;
C.发生AgCl(s)+I﹣(aq)AgI(s)+Cl﹣(aq),K= ![]() ,则
,则 ![]() <
< ![]() 时正向移动,即c(I﹣)=
时正向移动,即c(I﹣)= ![]() molL﹣1时,AgCl开始向AgI沉淀转化,故C错误;
molL﹣1时,AgCl开始向AgI沉淀转化,故C错误;
D.当Cl﹣开始沉淀时,c(Ag+)= ![]() =1.6×10﹣8mol/L,溶液中I﹣的浓度为
=1.6×10﹣8mol/L,溶液中I﹣的浓度为 ![]() =1.25×10﹣8 molL﹣1 , 故D正确;
=1.25×10﹣8 molL﹣1 , 故D正确;
故选D.


科目:高中化学 来源: 题型:
【题目】充分利用已有的数据是解决化学问题方法的重要途径.对数据的利用情况正确的是
A.利用化学平衡常数判断化学反应进行的快慢
B.利用溶解度数据判断氧化还原反应发生的可能性
C.利用沸点数据推测将一些液体混合物分离的可能性
D.利用物质的摩尔质量判断相同状态下不同物质密度的大小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2008年5月,我国四川地区发生特大地震灾害,地震过后,饮用水的消毒杀菌成为抑制大规模传染性疾病暴发的有效方法之一。氯气(Cl2)是制备消毒剂的主要原料之一。工业上主要采用电解饱和食盐水的方法来制取Cl2。请回答下列问题:
(1)电解之前,食盐水需要精制,目的是除去粗盐的中的Ca2+、Mg2+、SO42-等杂质离子,使用的试剂有:①Na2CO3溶液 ②Ba(OH)2溶液 ③稀盐酸。其中合理的加入顺序为___(填序号);
(2)实验室欲配制6.00 mol/L的食盐水90 mL,回答下列问题:
①需要纯净的NaCl___________________g。
②可供选择的仪器有:a玻璃棒 b烧瓶 c烧杯 d胶头滴管 e试管 f托盘天平、砝码 h药匙。在配制食盐水时不需要使用的有_______(填字母),还缺少的仪器是__________。
③配制溶液时,一般可以分为以下几个步骤:计算称量溶解(________________________)转移(_____________________)定容(__________________________)装瓶。
④下列操作会使所配溶液的浓度偏小的是___________________。
A. 转移完溶液后未洗涤玻璃棒和烧杯 B. 容量瓶中原来有少量蒸馏水
C. 定容时,俯视刻度线 D. 称量氯化钠固体时左码右物
(3)在电解饱和食盐水过程中,还生成了H2和NaOH,则所发生反应的化学反应方程式为_____________________________;
(4)将电解生成的Cl2通入NaOH溶液,生成两种盐,其中一种是消毒液的主要成分NaClO,应用氧化还原反应原理,写出此反应的化学方程式是_______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在50mL NaNO3和Na2SO4的混合溶液中,c (Na+)=1mol/L,往其中加入适量BaCl2溶液恰好完全反应,得到2.33g白色沉淀,则原混合溶液中c (NO3﹣)=mol/L.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温时,Ksp[Mg(OH)2]=1.1×10﹣11 , Ksp(AgCl)=1.8×10﹣10 , Ksp(Ag2CrO4)=1.9×10﹣12Ksp(CH3COOAg)=2.3×10﹣3 , 下列叙述不正确的是( )
A.浓度均为0.2 molL﹣1的AgNO3溶液和CH3COONa溶液等体积混合一定产生CH3COOAg沉淀
B.将0.001 molL﹣1的AgNO3溶液滴入0.001 molL﹣1的KCl和0.001 molL﹣1的K2CrO4的混合溶液中,先产生Ag2CrO4沉淀
C.c(Mg2+)为0.11 molL﹣1的溶液中要产生Mg(OH)2沉淀,溶液的pH要控制在9以上
D.在其他条件不变的情况下,向饱和AgCl水溶液中加入NaCl溶液,Ksp(AgCl)不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】取一定物质的量浓度的NaOH溶液100mL,然后向其通入一定量的CO2气体,得到溶液A,向A中逐滴缓慢加入0.1 molL-1的HCl溶液,产生的CO2气体体积(标准状况)与所加HCl溶液的体积之间关系如图所示,通过计算回答:
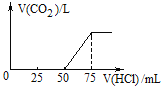
(1)A溶液中的溶质为_________(化学式),其物质的量之比是_______。
(2)通入CO2气体体积__________________(标准状况)。
(3)NaOH溶液的物质的量浓度______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,向20.00mL 0.1000molL﹣1 (NH4)2SO4溶液中逐滴加入0.2000molL﹣1 NaOH时,溶液的pH与所加NaOH溶液体积的关系如图所示(不考虑挥发).下列说法正确的是( ) 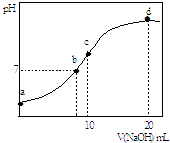
A.点a所示溶液中:c(SO42﹣)>c(NH4+)>c(H+)>c(OH﹣)
B.点b所示溶液中:c(NH4+)=c(Na+)>c(H+)=c(OH﹣)
C.点d所示溶液中:c(SO42﹣)>c(NH3H2O )>c(OH﹣)>c(NH4+)
D.点c所示溶液中:c(SO42﹣)+c(H+)=c(NH3H2O )+c(OH﹣)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】中国是中草药的发源地,目前中国大约有12000种药用植物,从某中草药提取的有机物结构如图所示,该有机物的下列说法中不正确的是( ) 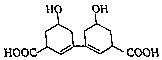
A.分子式为C14H18O6
B.环上氢原子的一氯取代物5种
C.1mol该有机物与足量的金属钠反应产生4mol H2
D.分子间能发生酯化反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com