
| A. | Al2(SO4)3 | B. | HCl | C. | Na2S | D. | NH3.H2O |
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:选择题
| A. | CaCl2 和 NaHS | B. | Na2O 和Na2O2 | C. | CO2 和HCl | D. | Na2O2 和NaOH |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Cl-,AlO2-,SO32-,Na+ | B. | NO3-,CH3COO-,Na+,NH4+ | ||
| C. | Cl-,NO3-,Mg2+,K+ | D. | SO42-,HCO3-,Cl-,K+ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 气体的浓度不再变化 | B. | 容器内压强不再改变 | ||
| C. | 气体的分子数不再变化 | D. | 各气体的浓度相等 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用托盘天平称取3.25gNaCl | |
| B. | 用量筒量取10.51mL盐酸 | |
| C. | 用酸式滴定管量取20.00mLKMnO4溶液 | |
| D. | 用容量瓶配制216mL0.1mol/L的NaOH溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 同浓度下列溶液中:①(NH4)2SO4 ②NH4HCO3 ③NH4Cl,④NH3•H2O,c(NH4+)由大到小的顺序是:①>③>②>④ | |
| B. | 常温时,将等体积的盐酸和氨水混合后pH=7,则c (NH4+)>c (Cl-) | |
| C. | 0.2 mol•L-1Na2CO3溶液中:c (CO32-)+c (HCO3-)+c (H2CO3)=0.2 mol•L-1 | |
| D. | 向醋酸钠溶液中加入适量醋酸,得到酸性溶液:c(Na+)>c(CH3COO-)>c(H+)>c(OH-) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1:1 | B. | 2:1 | C. | 1:2 | D. | 4:1 |
查看答案和解析>>
科目:高中化学 来源:2016-2017学年辽宁沈阳东北育才学校高二阶段考一化学卷(解析版) 题型:填空题
(1)氨的水溶液显弱碱性,其原因为 (用离子方程式表示),0.1 mol·L-1的氨水中加入少量的NH4Cl固体,溶液的PH (填“升高”或“降低”);若加入少量的明矾,溶液中的NH4+的浓度 (填“增大”或“减小”)。
(2)硝酸铵加热分解可得到N2O和H2O,250℃时,硝酸铵在密闭容器中分解达到平衡,该分解反应的化学方程式为 ,平衡常数表达式为 ;若有1mol硝酸铵完全分解,转移的电子数为 mol。
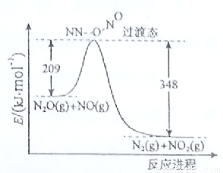
(3)由N2O和NO反应生成N2和NO2的能量变化如图所示,若生成1molN2,△H= kJ·mol-1。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com