
| A. | 室温下,1 L pH=12的氨水溶液中含有0.01NA个NH4+ | |
| B. | 1molFeCl3与沸水反应生成胶体后,含有NA个Fe(OH)3胶粒 | |
| C. | 常温常压下,11.2L O2和O3的混合气体含有0.5NA个分子 | |
| D. | 78g Na2O2固体中含有离子总数必为3NA |
分析 A、一水合氨为弱电解质;
B、一个氢氧化铁胶粒是多个氢氧化铁的聚集体;
C、常温常压下,气体摩尔体积大于22.4L/mol;
D、求出过氧化钠的物质的量,然后根据过氧化钠中含2个阳离子和1个阴离子构成.
解答 解:A、一水合氨为弱电解质,不能完全电离,故溶液中的铵根离子的个数小于0.01NA个,故A错误;
B、一个氢氧化铁胶粒是多个氢氧化铁的聚集体,故形成的胶粒个数小于NA个,故B错误;
C、常温常压下,气体摩尔体积大于22.4L/mol,故11.2L混合气体的物质的量小于0.5mol,则含有的分子个数小于0.5NA个,故C错误;
D、78g过氧化钠的物质的量为1mol,而过氧化钠中含2个阳离子和1个阴离子构成,故1mol过氧化钠中含3NA个离子,故D正确.
故选D.
点评 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.


 黄冈小状元解决问题天天练系列答案
黄冈小状元解决问题天天练系列答案 三点一测快乐周计划系列答案
三点一测快乐周计划系列答案科目:高中化学 来源: 题型:选择题
| A. | 加入盐酸,产生白色沉淀,则试样中一定有Ag+ | |
| B. | 加入盐酸,产生能使澄清石灰水变浑浊的无色气体,则试样中一定有CO32-或HCO3- | |
| C. | 加入NaOH溶液微热,产生使湿润红色石蕊试纸变蓝气体,则试样中一定有NH4+ | |
| D. | 加入BaCl2溶液,产生不溶于稀硝酸的白色沉淀,则试样中一定有SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | W、Y、Z三种元素的最高价氧化物的水化物可能有两种是强碱、一种是强酸 | |
| B. | Z元素在第三周期第ⅥA族 | |
| C. | W、Y、Z三种元素有两种是金属、一种是非金属 | |
| D. | W、X、Y三种元素的单质熔沸点依次降低 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在酸性条件下,CH3CO18 OC2H5的水解产物是CH3CO18OH和C2H5OH | |
| B. | 乙醛和丙烯醛不是同系物,它们与H2充分反应后的产物是同系物 | |
| C. | 用溴水可以鉴别苯酚溶液、2,4-己二烯、甲苯和CCl4 | |
| D. | 乳酸薄荷醇酯(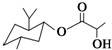 )能发生水解反应、氧化反应、消去反应、取代反应 )能发生水解反应、氧化反应、消去反应、取代反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
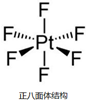 Ⅰ.一定条件下,O2可通过得失电子转化为O2-、O2+ 和O22-.
Ⅰ.一定条件下,O2可通过得失电子转化为O2-、O2+ 和O22-.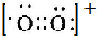 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题

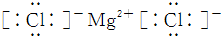 ;G的化学式为H2.
;G的化学式为H2.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 23 g Na与足量H2O反应完全后可生成NA个H2分子 | |
| B. | 1 mol Cu和足量热浓硫酸反应可生成NA个SO3分子 | |
| C. | 标准状况下,22.4 L N2和H2混合气中含NA个原子 | |
| D. | 3 mol单质Fe完全转变为Fe3O4,失去8NA个电子 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com