
【题目】(1)标况下,1.92g某气体的体积为672mL,则该气体的摩尔质量为 ;
(2)某金属氯化物为MCl29.5g,含有0.200molCl﹣ , 则该氯化物的摩尔质量 , 金属M的相对原子质量为 .
(3)71.5g碳酸钠晶体(Na2CO310H2O)溶于水,配成500ml溶液,此溶液的物质的量浓度为 .
(4)质量都是10g的HCl、NH3、CO2、H2四种气体在标准状况下,体积最小的是 ;密度最小的是 .(填化学式)
【答案】64g/mol;95g/mol;24;0.5mol/L;CO2;H2
【解析】(1)根据摩尔质量M=![]() =
=![]() =
=![]() =64g/mol,所以答案是:64g/mol;
=64g/mol,所以答案是:64g/mol;
(2)1molMCl2中含2mol氯离子,故含有0.200molCl﹣时,MCl2的物质的量为0.1mol,其摩尔质量M=![]() =
=![]() =95g/mol,金属M的相对原子质量为95﹣71=24,所以答案是:95g/mol,24;
=95g/mol,金属M的相对原子质量为95﹣71=24,所以答案是:95g/mol,24;
(3)71.5gNa2CO310H2O的物质的量n=![]() =0.25mol,而0.25molNa2CO310H2O中含0.25molNa2CO3 , 故溶液的物质的量浓度c=
=0.25mol,而0.25molNa2CO310H2O中含0.25molNa2CO3 , 故溶液的物质的量浓度c=![]() =
=![]() =0.5mol/L,所以答案是:0.5mol/L;
=0.5mol/L,所以答案是:0.5mol/L;
(4)当质量相同时,摩尔质量越大,物质的量越小,则在相同状态下体积越小,故体积最小的是CO2;密度和摩尔质量成正比,摩尔质量越大,密度越大,故密度最小的是 H2 . 所以答案是:CO2 , H2 .


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】下列现象与氢键有关的是( )
①NH3的熔、沸点比VA族其他元素氢化物的高
②乙醇、乙酸可以和水以任意比互溶
③冰的密度比液态水的密度小
④水分子高温下也很稳定.
A.①②③④
B.①②③
C.①②④
D.②③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据问题填空:
(1)下列各组物质: A.金刚石与石墨;B.淀粉与纤维素;C.氕与氘;D.甲烷与戊烷;E.葡萄糖与果糖
F. 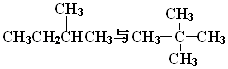 G.
G. 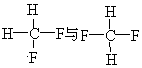
其中互为同位素的是(填编号,下同);互为同系物的是;互为同分异构体的是;是同一种物质的是 .
(2)化合物A的结构简式为: 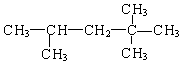 ,它是汽油燃烧品质抗震性能的参照物,其中A的同分异构体中含氢原子种类最少的一种结构简式为:;若A是由烯烃和H2通过加成反应得到,写出该烯烃的所有可能的结构简式 .
,它是汽油燃烧品质抗震性能的参照物,其中A的同分异构体中含氢原子种类最少的一种结构简式为:;若A是由烯烃和H2通过加成反应得到,写出该烯烃的所有可能的结构简式 .
(3)篮烷分子的键线式如图所示,试回答: 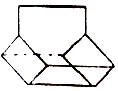
①写出篮烷分子的化学式;
②篮烷分子的一氯取代物的种数为种.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏伽德罗常数值,下列说法不正确的是( )
A.10 g D216O中所含中子数为5NA
B.标准状况下,22.4 L乙烷中所含共价键数目为7NA
C.7.8g Na2O2中所含阴、阳离子总数目为0.4NA
D.密闭容器中,1 mol N2和3 mol H2充分反应后,容器中的分子数一定大于2NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在汽车尾气处理装置中常发生如下反应:4CO+2NO2===4CO2+N2。下列对该反应的说法中正确的是
A. 该反应属于置换反应 B. 该反应中氧化剂是CO
C. 该反应NO2发生氧化反应 D. 该反应能减少汽车尾气对环境的污染
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】1997年,第一只“克隆羊”在英国诞生,“克隆羊”的关键技术之一是找到一些特殊的酶,它们能激活普通体细胞,使之像生殖细胞一样发育成个体.下列有关酶的叙述错误的是( )
A.酶是具有催化功能的蛋白质
B.酶的催化作用具有选择性和专一性
C.酶通常在强酸或强碱的条件下发挥作用
D.高温或紫外线的照射会降低酶的活性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有7种短周期元素的原子序数按A、B、C、D、E、F、G的顺序依次增大;B元素一种原子的含量常用于判定古生物遗体的年代,A和C元素的原子能形成4核10电子的微粒;D和E可形成离子化合物E2D,E2D中所有微粒的电子数相同,且电子总数为30;E、F、G的最高价氧化物对应的水化物之间可以相互反应;G和D同主族。试回答下列问题:
(1)C元素的原子结构示意图____________________。
(2)A和D可形成化合物的化学式为________。
(3)B元素在周期表中的位置为_____________;过量的B元素的最高价氧化物与氢氧化钠溶液反应的离子方程式为________________。
(4)D、E、F、G的离子半径由大到小顺序为(用离子符号表示)__________。
(5)F的单质与E元素的最高价氧化物对应的水化物反应的离子方程式为______,若将该反应设计成原电池,原电池的负极材料为___________。
(6)上述元素形成的二元化合物中,能够用于漂白的气体物质中含有的化学键类型为____,能够用于漂白的固体物质中阴、阳离子个数比为_________________。
(7)写出D元素原子形成的10电子微粒X与G元素原子形成的18电子微粒Y反应的离子方程式:_________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学实验小组,通过Li3N固体和水反应制取氨气,并进行氨气还原氧化铜的实验探究。如下图所示,给出了本实验可供选择的装置:

请回答下列问题:
(1)按该方法制氨气时,应选用上述装置中的______(填装置代码,下同)做氨气发生装置。写出Li3N和水反应制取氨气的化学方程式____________________。
(2)为检验氨气还原氧化铜反应后生成Cu、H2O、N2,氨气发生装置后应依次连接_____→C→____→_____。(给出的装置可重复使用)
(3)有资料提出:CuO被还原时,当黑色固体完全变为红时,不一定完全转化为Cu,可能还含有Cu2O.已知查阅到一离子反应方程式:Cu2O+2H+═Cu2++Cu+H2O.依据该信息,若要证明C处的红色固体中是否含有Cu2O,请设计实验:_____________________________ 。
(4)甲同学认为利用上述实验设计改进后的装置还可测定Cu的相对原子质量,他是通过测定反应物CuO的质量和生成物H2O的质量来完成的。若实验测得完全反应的CuO和生成的H2O的质量分别为m(CuO)、m(H2O),则据此计算Cu的相对原子为______。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com