
| A、五种元素的原子半径从大到小的顺序是:M>W>Z>Y>X |
| B、X、Z两元素能形成原子个数比(X:Z)为3:1和4:2的化合物 |
| C、化合物YW2、ZW2都是酸性氧化物 |
| D、用M单质作阳极,石墨作阴极电解NaHCO3溶液,电解一段时间后,在阴极区会出现白色沉淀 |


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
 TiO2在光照下可使水分解:2H2O
TiO2在光照下可使水分解:2H2O
| ||
| 光 |
| A、该装置可以将光能转化为电能,同时电能转化为化学能 |
| B、铂电极上发生的反应为:2H++2e-=H2↑ |
| C、该装置工作时,电流由TiO2电极流向铂电极 |
| D、该装置工作时,TiO2电极附近溶液的pH变小 |
查看答案和解析>>
科目:高中化学 来源: 题型:
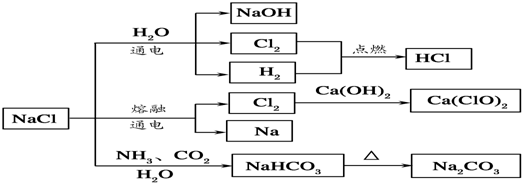
| A、25℃,NaHCO3在水中的溶解度比Na2CO3的大 |
| B、石灰乳和Cl2反应可制得漂白粉,其主要成分是次氯酸钙 |
| C、常温下干燥的Cl2能用钢瓶贮存,所以Cl2不与铁反应 |
| D、如图所示转化反应不都是氧化还原反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
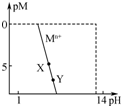 常温下,一些金属离子(用Mn+表示)形成M(OH)n沉淀与溶液pH平衡关系曲线如图.已知:c(Mn+)≤1×10-5mol?L-1时可认为金属离子沉淀完全;pM=-lgc(Mn+),pKsp=-lgKsp.下列叙述正确的是( )
常温下,一些金属离子(用Mn+表示)形成M(OH)n沉淀与溶液pH平衡关系曲线如图.已知:c(Mn+)≤1×10-5mol?L-1时可认为金属离子沉淀完全;pM=-lgc(Mn+),pKsp=-lgKsp.下列叙述正确的是( )| A、Mn+ 开始沉淀的pH与起始溶液c(Mn+)无关 |
| B、不同的金属沉淀完全时的pH相同 |
| C、图中Y点与X点pKsp相同 |
| D、Y点:pM=pKsp+npH-14n |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、0.375mol |
| B、0.15mol |
| C、1.375mol |
| D、1.5mol |
查看答案和解析>>
科目:高中化学 来源: 题型:

| A、X可能含有2种盐 |
| B、a是SO3 |
| C、Y可能含有(NH4)2SO4 |
| D、(NH4)2S2O8中S的化合价不可能为+7 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、每生成1mol Fe3O4,反应转移的电子总数为2mol | ||
| B、Fe2+和S2O32-都是还原剂 | ||
C、1mol Fe2+被氧化时,被Fe2+还原的O2的物质的量为
| ||
| D、x=4 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com