
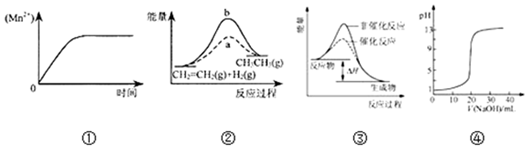
| A�� | ͼ�ٱ�ʾ10 mL 0.01 mol•L-1 KMnO4 ������Һ�������0.1 mol•L-1 H2C2O4��Һ�� ��ʱ��n��Mn2+�� ��ʱ��ı仯 | |
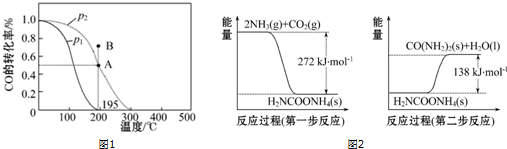
| B�� | ͼ����a��b���߷ֱ��ʾ��ӦCH2=CH2 ��g��+H2��g����CH3CH3��g������H��0ʹ�ú�δʹ�ô���ʱ����Ӧ�����е������仯 | |
| C�� | ͼ�۱�ʾij���ȷ�Ӧ�ֱ����С�����������·�Ӧ�����е������仯 | |
| D�� | ͼ�ܱ�ʾ0.1000mol•L-1NaOH��Һ�ζ�20.00mL0.1000mol•L-1CH3COOH��Һ���õ��ĵζ����� |
���� A��n��Mn2+����ʼΪ0���淴Ӧ�ķ���������������ԭ��Ӧ�����������ʵ������ٱ仯��
B����Ӧ��������������������������ӦΪ���ȷ�Ӧ��
C��������������ͷ�Ӧ�Ļ�ܣ�
D.0.1000mol•L-1CH3COOH��ҺpH��1��
��� �⣺A��n��Mn2+����ʼΪ0���淴Ӧ�ķ�����������Ũ������Ϊ��Ӧ�Ĵ�������Ӧ��������������ԭ��Ӧ�����������ʵ������ٱ仯������б�ʿ�ʼ��С����ͻȻ����A����
B����Ӧ��������������������������ӦΪ���ȷ�Ӧ�����H��0����B����
C��������������ͷ�Ӧ�Ļ�ܣ���C��ȷ��
D������Ϊ���ᣬ������ȫ���룬0.1000mol•L-1CH3COOH��ҺpH��1����D����
��ѡC��
���� ���⿼���Ϊ�ۺϣ�Ϊ�߿��������ͣ�������ѧ���ķ��������Ŀ��飬ע����շ�Ӧ�е������仯��ͼ��ĺ��弴�ɽ�𣬶�ѧ������Ҫ��ϸߣ��Ѷ��еȣ�


 һ����ʦ�����Ծ�ϵ�д�
һ����ʦ�����Ծ�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| t/min | 0 | 1 | 3 | 5 |
| n��H2��/mol | 8 | 5 | 4 | 4 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
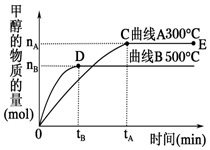 һ�������£����ݻ�Ϊ3L���ܱ������У�������ӦCO��g��+2H2��g��?CH3OH��g����H��0���ڲ�ͬ�¶��¼״������ʵ�����ʱ��ı仯��ͼ��ʾ������������ȷ���ǣ�������
һ�������£����ݻ�Ϊ3L���ܱ������У�������ӦCO��g��+2H2��g��?CH3OH��g����H��0���ڲ�ͬ�¶��¼״������ʵ�����ʱ��ı仯��ͼ��ʾ������������ȷ���ǣ�������| A�� | ƽ�ⳣ��K��300�棩��K��500�棩 | |
| B�� | 500�棬�ӷ�Ӧ��ʼ��ƽ�⣬������ƽ����Ӧ����v��H2��=$\frac{nB}{3tB}$ mol•L-1•min-1 | |
| C�� | �������������������£�������E�����ϵ���ݻ�ѹ����ԭ����$\frac{1}{2}$��������Ũ�ȼ�С | |
| D�� | 300�棬��������ѹǿ����ʱ˵����Ӧ�Ѿ��ﵽƽ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
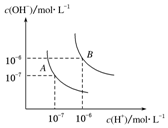 ˮ�ĵ���ƽ��������ͼ��ʾ����A���ʾ25��ʱˮ�ĵ����ƽ��ʱ������Ũ�ȣ�B���ʾ100��ʱˮ�ĵ����ƽ��ʱ������Ũ�ȣ���100��ʱ1mol•L-1��NaOH��Һ�У���ˮ�������c��H+��=1��10-12mol•L-1��KW��25�棩��KW��100�棩�����������������=������
ˮ�ĵ���ƽ��������ͼ��ʾ����A���ʾ25��ʱˮ�ĵ����ƽ��ʱ������Ũ�ȣ�B���ʾ100��ʱˮ�ĵ����ƽ��ʱ������Ũ�ȣ���100��ʱ1mol•L-1��NaOH��Һ�У���ˮ�������c��H+��=1��10-12mol•L-1��KW��25�棩��KW��100�棩�����������������=�������鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
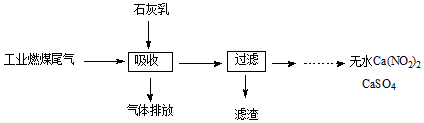
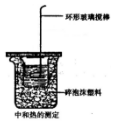 ijͬѧ����ͼװ�����к��ȵIJⶨʵ��
ijͬѧ����ͼװ�����к��ȵIJⶨʵ���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | O2�ǻ�ԭ�� | B�� | NH3�������� | C�� | O2�õ����� | D�� | NH3������ԭ��Ӧ |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com