
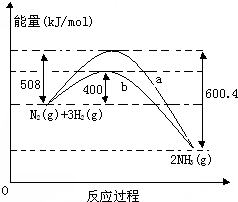
 如图表示常温常压下N2(g)与H2(g)反应生成NH3(g)过程中的能量变化曲线,a和b表示不同条件下反应过程中的能量变化曲线.
如图表示常温常压下N2(g)与H2(g)反应生成NH3(g)过程中的能量变化曲线,a和b表示不同条件下反应过程中的能量变化曲线.

 云南师大附小一线名师提优作业系列答案
云南师大附小一线名师提优作业系列答案 冲刺100分单元优化练考卷系列答案
冲刺100分单元优化练考卷系列答案科目:高中化学 来源: 题型:
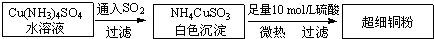
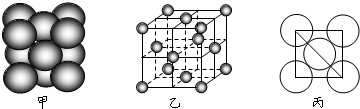
查看答案和解析>>
科目:高中化学 来源: 题型:
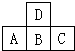 如图中A、B、C、D是短周期中同周期或同主族的相邻元素.
如图中A、B、C、D是短周期中同周期或同主族的相邻元素.查看答案和解析>>
科目:高中化学 来源: 题型:
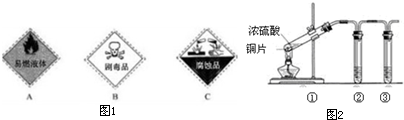
查看答案和解析>>
科目:高中化学 来源: 题型:
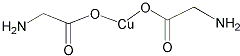
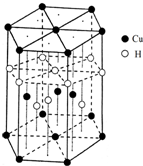
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、将SO2通入BaCl2溶液可生成BaSO3沉淀 |
| B、Na2O、Na2O2组成元素相同,与 CO2反应产物也相同 |
| C、H2CO3的酸性比HClO弱,推出CO2通入NaClO溶液中不能生成HClO |
| D、SiO2是酸性氧化物,能与NaOH溶液反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、稀醋酸加水稀释,醋酸电离程度增大,溶液的pH升高 |
| B、在CH3COONa溶液中加入适量CH3COOH,可使c(Na+)=c(CH3COO-) |
| C、在含有BaSO4沉淀的溶液中加入Na2SO4固体,溶液中c(Ba2+)减小 |
| D、常温下,pH=2的盐酸与pH=12的氨水等体积混合所得溶液c(H+)>c(OH-) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com