
(10分)在含有弱电解质的溶液中,往往有多个化学平衡共存。
(1)一定温度下,向1 L 0.1 mol·L-1CH3COOH溶液中加入0.1 mol CH3COONa固体,溶液中
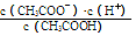 (填“增大”、“减小”或“不变”);写出表示该混合溶液中所有离子浓度之间的一个等式 。
(填“增大”、“减小”或“不变”);写出表示该混合溶液中所有离子浓度之间的一个等式 。
(2)土壤的pH一般在4~9之间。土壤中Na2CO3含量较高时,pH可以高达10.5,试用离子方程式解释土壤呈碱性的原因 。加入石膏(CaSO4·2H2O)可以使土壤碱性降低,有关反应的化学方程式为 。
(3)常温下向20 mL 0.1 mol·L-1Na2CO3溶液中逐滴加入0.1 mol·L-1HCl溶液40 mL,溶液中含碳元素的各种微粒(CO2因逸出未画出)物质的量分数随溶液pH变化的情况如下:
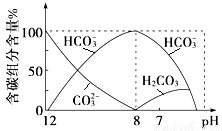
回答下列问题:
①在同一溶液中,H2CO3、HCO3-、CO32- (填“能”或“不能”)大量共存;
②当pH=7时,溶液中含碳元素的主要微粒有 、 ,溶液中含量最多的三种微粒的物质的量浓度的大小关系为 ;
(1)不变(1分)c(CH3COO-)+c(OH-)=c(H+)+c(Na+)(2分)
(2) CO32-+H2O HCO3-+OH-(2分)
HCO3-+OH-(2分)
Na2CO3+CaSO4·2H2O===CaCO3+Na2SO4+2H2O或
Na2CO3+CaSO4===CaCO3+Na2SO4(2分)
(3)①不能(1分)
②HCO3-、H2CO3(2分) c(Na+)>c(Cl-)>c(HCO3-)(2分)
【解析】
试题分析:(1)电离平衡常数Ka=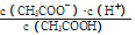 ,只受温度的影响,温度不变Ka不变;电解质溶液中电荷守恒式c(CH3COO-)+c(OH-)=c(H+)+c(Na+)中含有溶液中的所有离子。
,只受温度的影响,温度不变Ka不变;电解质溶液中电荷守恒式c(CH3COO-)+c(OH-)=c(H+)+c(Na+)中含有溶液中的所有离子。
(2)Na2CO3为强碱弱酸盐水解呈碱性,加入石膏(CaSO42H2O)生成碳酸钙沉淀,使CO32-浓度降低,水解平衡左移,c(OH-)减小,土壤碱性降低。(3).常温下向Na2CO3溶液中逐滴加入HCl溶液反应顺序为:
Na2CO3+HCl=NaHCO3+ NaCl
NaHCO3+HCl=NaCl+CO2↑+H2O
在同一溶液中,因CO2+H2O +CO32-=2 HCO3-,所以H2CO3 、HCO3-、CO32-不能大量共存;
由图象可知,当pH=7时,碳元素存在于HCO3-、H2CO3中,且c(HCO3-)>c(H2CO3),根据c(Na+)+c(H+)=c(Cl-)+c(HCO3-)+c(OH-)及c(H+)=c(OH-)可得c(Na+)>c(Cl-),又由于HCO3-水解c(Cl-)>c(HCO3-),所以主要的三种离子大小顺序为c(Na+)>c(Cl-)>c(HCO3-)。
考点:了解弱电解质在水溶液中的电离平衡。了解盐类水解的原理、影响盐类水解程度的主要因素、盐类水解的应用。


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源:2014-2015学年安徽省安庆五校联盟高三下学期3月联考理综化学试卷(解析版) 题型:选择题
常温下,在下列给定条件的各溶液中,一定能大量共存的离子组是
A.PH大于7的溶液:Na+、Ba2+、SO32-、ClO—
B.含有0.1 mol·L-1 Fe(NO3)2的溶液:H+、Mg2+、SCN-、Cl-
C.使酚酞试液变红色的溶液:Na+、Ba2+、I-、Cl-
D.由水电离产生的c(H+)=10-13mol·L-1的溶液:NH4+、SO42-、NO3-、Cl-
查看答案和解析>>
科目:高中化学 来源:2014-2015学年山东省济南市高三上学期期末考试化学试卷(解析版) 题型:选择题
实验室需配制一种溶液,除水电离出的离子外还含有五种离子,且在该溶液中这五种离子的物质的量浓度均为l mol·L-1,下面四个选项中,能达到此要求的是
A.Al3+、K+、SO42-、Cl-、HCO3- B.Fe2+、H+、Br-、NO3—、Cl-
C.Na+、K+、SO42-、NO3—、Cl- D.Al3+、Na+、Cl-、SO42-、NO3—
查看答案和解析>>
科目:高中化学 来源:2014-2015学年湖北大冶一中等六校高三元月调考理综化学试卷(解析版) 题型:实验题
(15分)硫代硫酸钠是一种重要的化工产品。工业上常利用含硫废水生产Na2S2O35H2O,实验室可用如下装置(略去部分加持仪器)模拟生成过程。
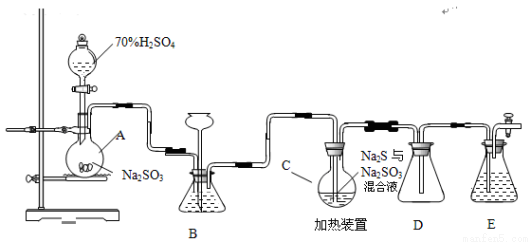
烧瓶C中发生反应如下:
Na2S(aq)+H2O(l)+SO2(g)=Na2SO3(aq)+H2S(aq) (I)
2H2S(aq)+SO2(g)=3S(s)+2H2O(l) (II)
S(s)+Na2SO3(aq) Na2S2O3(aq) (III)
Na2S2O3(aq) (III)
(1)仪器组装完成后,关闭两端活塞,向装置B中的长颈漏斗内注入液体至形成一段液注,若 ,则整个装置气密性良好。装置D的作用是 。装置E中为 溶液。
(2)为提高产品纯度,应使烧瓶C中Na2S和Na2SO3恰好完全反应,则烧瓶C中Na2S和Na2SO3物质的量之比为 。
(3)装置B的作用之一是观察SO2的生成速率,其中的液体最好选择 。
a.蒸馏水 b.饱和Na2SO3溶液
c.饱和NaHSO3溶液 d.饱和NaHCO3溶液
(4)实验中,为使SO2缓慢进入烧瓶C,采用的操作是 。
(5)已知反应(III)相对较慢,则烧瓶C中反应达到终点的现象是 。
(6)反应终止后,烧瓶C中的溶液经蒸发浓缩冷却,过滤,洗涤,干燥,即得到粗产品(主要含有Na2S2O35H2O和其他杂质)。某兴趣小组为测定该产品纯度,准确称取4.96 g产品,用适量蒸馏水溶解,以淀粉作指示剂,用0.1000 molL1碘的标准溶液滴定。反应原理为:2S2O32-+I2=S4O62-+2I,滴定至终点时,滴定起始和终点的液面位置如下图,则产品的纯度为_________。
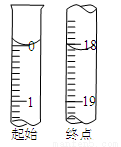
经仪器分析,该产品纯度为16%,分析该兴趣小组测定产品纯度偏差的原因(忽略人为误差)_______。
[M(Na2S2O35H2O)=248g/mol]
查看答案和解析>>
科目:高中化学 来源:2014-2015学年湖北大冶一中等六校高三元月调考理综化学试卷(解析版) 题型:选择题
下列离子方程式书写正确的是
A.H218O中投入Na2O2固体:2H218O+2Na2O2===4OH-+4Na++18O2↑
B.Fe3O4与稀HNO3反应:Fe3O4+8H+===Fe2++2Fe3++4H2O
C.向NaHCO3溶液中加入少量Ca(OH)2:HCO3-+Ca2++OH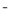 ===CaCO3↓+H2O
===CaCO3↓+H2O
D.将少量NaOH溶液加入到NH4HCO3溶液中:OH-+HCO3-===CO32-+H2O
查看答案和解析>>
科目:高中化学 来源:2014-2015学年河南省高三12月月考化学试卷(解析版) 题型:选择题
下列实验对应的结论不正确的是

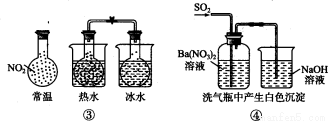
A.①能组成Zn-Cu原电池
B.②能证明非金属性Cl>C>Si
C.③能说明 △H<0
△H<0
D.④中自色沉淀为BaS04
查看答案和解析>>
科目:高中化学 来源:2014-2015学年河南省高三12月月考化学试卷(解析版) 题型:选择题
镁粉是制备焰火的原料,工业上通过冷却镁蒸气制得镁粉。下列气体中可以用冷却镁蒸气的是
A.空气 B.二氧化碳 C.氧气 D.氩气
查看答案和解析>>
科目:高中化学 来源:2014-2015学年安徽省六校教育研究会高三联考化学试卷(解析版) 题型:选择题
下列表示对应化学反应的离子方程式正确的是
A.向NaHCO3溶液中加入过量的澄清石灰水,出现白色沉淀:2HCO3-+Ca2++2OH-=CaCO3↓+CO32-+2H2O
B.向NH4HCO3溶液中加过量NaOH溶液并加热:NH4++OH-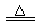 NH3↑+H2O
NH3↑+H2O
C.将过量二氧化硫气体通入氨水中:SO2+NH3·H2O=HSO3-+NH4+
D.用稀硝酸洗涤试管内壁的银镜:Ag+2H++3NO3-=Ag++NO↑+H2O
查看答案和解析>>
科目:高中化学 来源:2014-2015四川省攀枝花市高一上学期期末考试化学试卷(解析版) 题型:填空题
(6分)标出下列氧化还原反应的电子转移数目和方向,并写出氧化剂和还原剂
(1)2MnO2 + 4KOH + O2  2K2MnO4 + 2H2O
2K2MnO4 + 2H2O
氧化剂是 ,还原剂是
(2)3NaClO3 +10HCl(浓) 3NaCl + 4Cl2↑+ 2ClO2↑ + 5H2O
3NaCl + 4Cl2↑+ 2ClO2↑ + 5H2O
氧化剂是 ,还原剂是
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com