
���� ��1����ԭ�������ܶ�Ϊ1.25g/L����״��������ԭ������ƽ�����Ħ������Ϊ1.25g/L��22.4L/mol=28g/mol�����ݰ�����Ħ������Ϊ17g/mol��������Ħ������Ϊ29g/mol������ƽ��ֵ����ȷ�����ǵ�����ȣ�
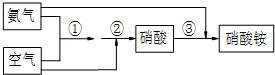
��2������������İ���������е�����ǡ����ȫ��Ӧ���������������ʵ��������÷�Ӧ4NH3+5O2=4NO+6H2O�ͷ�Ӧ4NO+3O2+2H2O=4HNO3����ȷ����Ӧ�����ɵ�ˮ�����ʵ��������õ�Ԫ���غ�ɼ����������������ʵ���������ȷ������������Һ�����ʵ���Ũ�ȣ�
��3���������Ǹ���Ӧ�Ҹ�����Ӧ����ȫ�����������в��ٲ����������ɽ���Ӧ4NH3+5O2=4NO+6H2O�ͷ�Ӧ4NO+3O2+2H2O=4HNO3��NH3+HNO3=NH4NO3 �ϲ���2NH3+2O2=NH4NO3+H2O���ݴ˿ɼ������������������������ȣ�����������ռ$\frac{1}{5}$���ݴ˿ɼ����ԭ�����а��������������
��4����i������100m3��������x������ȡHNO3����1-x����HNO3���գ����ݷ�ӦNH3+HNO3��NH4NO3�ɼ���x��ֵ�����������100m3�������㵽��״��������������������淋�������
��ii���������з�Ӧ�е�ϵ���ɼ���ڢٲ��μӷ�Ӧ�İ�Ϊ4mol�����������������n��HNO3��=4��0.94��0.97��mol�����ڢ۲���Ҫ��������n��NH3��=n��HNO3��/0.98=��4��0.94��0.97��/0.98��mol��������ת����=$\frac{��ת�������ʵ���}{��ʼ���ʵ���}$��100%����ϳ�����淋����������а�����ת���ʣ�
��� �⣺��1����ԭ�������ܶ�Ϊ1.25g/L����״��������ԭ������ƽ�����Ħ������Ϊ1.25g/L��22.4L/mol=28g/mol�����ݰ�����Ħ������Ϊ17g/mol��������Ħ������Ϊ29g/mol���谱��������������Ϊx��y������$\frac{17x+29y}{x+y}$=28������x��y=1��11��
�ʴ�Ϊ��1��11��
��2������������İ���������е�����ǡ����ȫ��Ӧ�����谱�������ʵ���Ϊ4mol������ݷ�Ӧ4NH3+5O2=4NO+6H2O�ͷ�Ӧ4NO+3O2+2H2O=4HNO3����֪��Ӧ�����ɵ�ˮ�����ʵ���Ϊ4mol��ͬʱ��������Ϊ4mol����������������Һ������Ϊ4��18g+63��4g=324g��������Һ�����Ϊ$\frac{324g}{1.38g/c{m}^{3}}$=0.235L������������ʵ���Ũ��Ϊ$\frac{4mol}{0.235L}$=17.02mol/L��
�ʴ�Ϊ��17.02mol/L��
��3���������Ǹ���Ӧ�Ҹ�����Ӧ����ȫ�����������в��ٲ����������ɽ���Ӧ4NH3+5O2=4NO+6H2O�ͷ�Ӧ4NO+3O2+2H2O=4HNO3��NH3+HNO3=NH4NO3 �ϲ���2NH3+2O2=NH4NO3+H2O���������������������Ϊ1��1������������ռ$\frac{1}{5}$����ԭ�����а������������Ϊ$\frac{1}{6}$��100%=16.67%��
�ʴ�Ϊ��16.67%��
��4����i������100m3������������ȡHNO3�İ����ķ���Ϊx����HNO3���յİ����ķ���Ϊ��1-x�������ɵ������Ϊy��
���ݷ�ӦNH3+HNO3��NH4NO3��100��103����1-x����98%=100��103��x��94%��97%������x=0.52����y=169334��g��=169��kg����
�ʴ�Ϊ��169��
��ii���������з�Ӧ�е�ϵ���ɼ���ڢٲ��μӷ�Ӧ�İ�Ϊ4mol����������ʼ�����ʵ���Ϊ4mol+��4��0.94��0.97��/0.98mol�����������������n��HNO3��=4��0.94��0.97��mol�����ڢ۲���Ҫ��������n��NH3��=n��HNO3��/0.98=��4��0.94��0.97��/0.98��mol����������ת����=$\frac{��ת�������ʵ���}{��ʼ���ʵ���}$��100%=$\frac{4mol+4��0.94��0.97mol}{4mol+��4��0.94��0.97��/0.98mol}$��100%=94.47%��
�𣺰���ת����Ϊ94.47%��
���� ���⿼����������Ĺ�ҵ�Ʊ����̱����µĻ�ѧ���㣬�ؼ������ݸ�����ԭ�ϺͲ����Ĺ�ϵ��������ʽ��������ʽ������Ӧ����Ԫ������Ŀ�����ʵĹ�ϵ����Ŀ�Ѷ��еȣ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
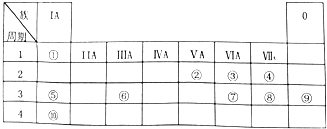
 ��Ԫ�ؿ��γ�±����������P�����ȣ�
��Ԫ�ؿ��γ�±����������P�����ȣ��鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����

| A�� | 2-�һ�-4-�촼 | B�� | 4-��-2-�Ѵ� | C�� | 4-�һ�-2-�촼 | D�� | 3-��-5-�Ѵ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
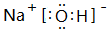 ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
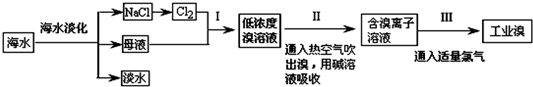
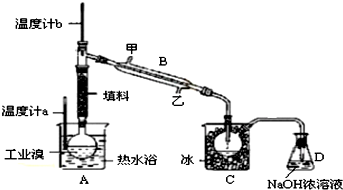
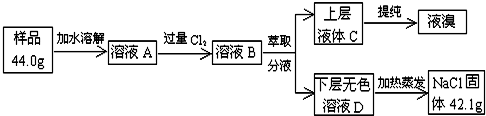
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 2������ | B�� | 20�˵Ķ������� | C�� | 46�˵Ľ����� | D�� | 3Ħ����ˮ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ������ˮ���γɵ���Һ�� | |
| B�� | �����ܣ�Co2O2����ɢ����ͨ�������γ���ɫ�л����� | |
| C�� | ����FeCl3��Һ�����ˮ�����γɵĺ��ɫҺ�� | |
| D�� | ��0.1g���Ǽӵ�10mL����ˮ�У����γɵ���ɫҺ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ��Ч��������������Դ�Ϳ�������Դ���ܵ����������ӣ�
��Ч��������������Դ�Ϳ�������Դ���ܵ����������ӣ��鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com