
催化剂在生产和科技领域起到重大作用。为比较Fe3+和Cu2+对H2O2分解的催化效果,某化学研究小组的同学分别设计了如图甲、乙所示的实验。请回答相关问题:

⑴ 定性分析:如图甲可通过观察 ,定性比较得出结论。同学X观察甲中两支试管产生气泡的快慢,由此得出Fe3+和Cu2+对H2O2分解的催化效果,其结论________(填“合理”或“不合理”),理由是 。
⑵ 定量分析:如图乙所示,实验时均以生成40 mL气体为准,其它可能影响实验的因素均已忽略。实验中检验气密性的方法是
,需要测量的数据是 。
 ⑶ 加入0.10 mol MnO2粉末于50 mL H2O2溶液中,在标准状况下放出气体的体积和时间的关系如右图所示。
⑶ 加入0.10 mol MnO2粉末于50 mL H2O2溶液中,在标准状况下放出气体的体积和时间的关系如右图所示。
① 实验时放出气体的总体积是 mL。
② 放出1/3气体所需时间为 min。
③ 计算H2O2的初始物质的量浓度 。 (请保留两位有效数字)
④ A、B、C、D各点反应速率快慢的顺序为_______>______>______>______。
⑤ 解释④反应速率变化的原因___ 。
科目:高中化学 来源: 题型:
下列说法正确的是( )
A. 同温同压下, 在光照和点燃条件下的反应热不同
在光照和点燃条件下的反应热不同
B. 反应: ,使用和未使用催化剂时,反应热不同
,使用和未使用催化剂时,反应热不同
C. 用硝酸这一种试剂就能将 、
、 、Na2CO3、
、Na2CO3、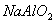 四种溶液鉴别出来
四种溶液鉴别出来
D. 依据丁达尔现象就可将分散系分为溶液、胶体与浊液
查看答案和解析>>
科目:高中化学 来源: 题型:
正长石的主要成分为硅酸盐,由前20号元素中的4种组成,化学式为XYZ3W8。其中,只有W显负价。X、Y的最外层电子数之和与Z的最高正价数相等。Y3+与W的阴离子具有相同的电子层结构。X、W的质子数之和等于Y、Z的质子数之和。下列说法错误的是( )
A.X的离子半径>Y的离子半径
B.Z的氢化物的稳定性<W的氢化物的稳定性
C.Y的氧化物既能与盐酸反应,又能与NaOH溶液反应
D.X2W2、Y2W3两种化合物含有的化学键类型完全相同
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关说法中,正确的是( )
A.分馏、干馏、裂化都是化学变化 B.聚乙烯、聚氯乙烯、纤维素都是合成高分子
C.硫酸铜、醋酸、铁都是电解质 D.盐酸、漂白粉、铝热剂都是混合物
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于有机物的说法错误的是( )
A.由CH2=CHCOOCH3合成的聚合物为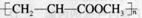
B.溴乙烷与NaOH乙醇溶液共热生成乙烯 C.装饰材料中的甲醛和芳香烃会造成居室污染
D.磨豆浆的大豆富含蛋白质,豆浆煮沸后蛋白质变成了氨基酸
查看答案和解析>>
科目:高中化学 来源: 题型:
在复杂的体系中,确认化学反应先后顺序有利于解决问题,下列化学反应先后顺序判断正确的是( )
A.含等物质的量的AlO2-、OH-、CO32-的溶液中,逐滴加入盐酸:AlO2-、OH-、CO32-
B.含等物质的量的FeBr2、FeI2的溶液中 ,缓慢通入氯气:I-、Br-、Fe2+
,缓慢通入氯气:I-、Br-、Fe2+
C.含等物质的量的Ba(OH)2、KOH的溶液中,缓慢通入CO2:KOH、Ba(OH) 2、K2CO3、BaCO3
2、K2CO3、BaCO3
D.含等物质的量的Fe3+、Cu2+、H+的溶液中加入锌粉:Fe3+、Cu2+、H+、Fe2+
查看答案和解析>>
科目:高中化学 来源: 题型:
离子液体是一种室温熔融盐,为非水体系。由有机阳离子、Al2Cl 和AlCl
和AlCl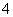 组成的离子液体作电解液时,可在钢制品上电镀铝。
组成的离子液体作电解液时,可在钢制品上电镀铝。
(1)钢制品接电源的________极,已知电镀过程中不产生其他离子且有机阳离子不参与电极反应,阴极电极反应式为__________________________________________。若改用AlCl3水溶液作电解液,则阴极产物为________。
(2)为测定镀层厚度,用NaOH溶液溶解钢制品表面的铝镀层,当反应转移6 mol电子时,所得还原产物的物质的量为________mol。
(3)用铝粉和Fe2O3做铝热反应实验,需要的试剂还有________。
a.KCl b.KClO3 c.MnO2 d.Mg
取少量铝热反应所得的固体混合物,将其溶于足量稀H2SO4,滴加KSCN溶液无明显现象,______________(填“能”或“ 不能”)说明固体混合物中无Fe2O3,理由是________(用离子方程式说明)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com