

���� ��1������˫��ˮ��������һ����ʽ�κ�һ����ʹʪ��ĺ�ɫʯ����ֽ���������壬�������غ㶨�ɿ�֪������̼�����ƺͰ�����
�����ӷ���ʽΪCN-+S2O32-=A+SO32-����ϵ���غ㡢ԭ���غ������
��2��������������ClO-����������ʧȥ���ӣ�
��ClO-��CN-����Ϊ��������Ⱦ�����壬���ɵ����Ͷ�����̼��
��3��˫��ˮ��̼���ƻ�Ͽ����¶ȷ�����Ӧ2Na2CO3 ��aq��+3H2O2 ��aq��?2Na2CO3•3H2O2��s�������ù��˵õ�����2Na2CO3•3H2O2��������ϴ�ӡ�����õ��ϴ�����2Na2CO3•3H2O2��
�ٹ�̼�����൱�ڴ��ᾧ˫��ˮ��̼���ƣ�����˫��ˮ�����ʣ���������ԭ�������״ٽ���̼���Ʒ�Ӧ������ʧЧ��
����д����Ӧ�Ļ�ѧ����ʽ��Ȼ�����˫��ˮ�������ص����ʵ�����ϵ�������Ʒ��˫��ˮ�İٷֺ�����
��� �⣺��1������˫��ˮ�����軯�ƣ�����һ����ʹʪ��ĺ�ɫʯ����ֽ����������Ϊ��������ԭ���غ��֪��ʽ��Ϊ̼�����ƣ���ӦΪNaCN+H2O2+H2O�TNaHCO3+NH3����
�ʴ�Ϊ��NaCN+H2O2+H2O�TNaHCO3+NH3����
��CN-+S2O32-�TA+SO32-�����ݵ���غ㣬AΪ-1�۵������ӣ�����ԭ���غ㣬A�к���1����ԭ�ӡ�1��̼ԭ�ӡ�1����ԭ�ӣ���AΪSCN-���ʴ�Ϊ��SCN-��
��2��������������ClO-����������ʧȥ���ӣ��缫��ӦΪ2OH-+Cl--2e-�TClO-+H2O���ʴ�Ϊ��2OH-+Cl--2e-�TClO-+H2O��
��ClO-��CN-����Ϊ��������Ⱦ�����壬���ɵ����Ͷ�����̼���ɵ��ӡ�����غ��֪ȥ��CN-�����ӷ���ʽΪ2CN-+H2O+5ClO-�T5Cl-+N2��+2OH-+2CO2����
�ʴ�Ϊ��2CN-+H2O+5ClO-�T5Cl-+N2��+2OH-+2CO2��
��3���ٹ�̼�����൱�ڴ��ᾧ˫��ˮ��̼���ƣ�����˫��ˮ�����ʣ�FeCl3����˫��ˮ�ֽ�Ĵ�����KCN���л�ԭ�ԣ��ܱ���̼����������CuSO4��˫��ˮ�ķֽ⣬�����Ʋ����̼���Ʒ�Ӧ��
�ʴ�Ϊ��C��
��KMnO4Ϊ��ɫ���۲���ζ�ʱ��ɫ�仯���жϵζ��յ㣬����Ҫָʾ����
���������Һ���̼���Ʒ�Ӧ�Ļ�ѧ����ʽΪ��6KMnO4+5��2Na2CO3•3H2O2��+19H2SO4�T3K2SO4+6MnSO4+10Na2SO4+10CO2��+15O2��+34H2O���ζ�����������2.000x10-2 mol•L-1 KMnO4����Һ�����ʵ���Ϊ��2.000x10-2 mol•L-1��0.03L=6.000x10-4mol��
��������������Ϊxg�����ݹ�ϵʽ
KMnO4��2Na2CO3•3H2O2��15H2O2
6mol 15��34g
6.000��10-4mol x
���x=0.051
�����������������Ϊ$\frac{0.051g}{0.2g}$=25.50%��
�ʴ�Ϊ����25.50%��
���� ���⿼����������ᴿ����������ȣ��ۺ��Խ�ǿ������ϰ���е���Ϣ��������ԭ��Ӧ���غ㷨Ӧ�õ�Ϊ���Ĺؼ������ط��������������Ŀ��飬��Ŀ�Ѷ��еȣ�


 �ܿ�����ĩ��̾�ϵ�д�
�ܿ�����ĩ��̾�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| ʵ����� | ʵ�鲽�裨���ݣ� | ���� |
| �� | �����б�ǩa��b���Թ��зֱ����1.0 g Na2CO3�����NaHCO3���壬�۲���ۣ� | / |
| �� | �ֱ���뼸��ˮ�������Թܵײ��� | �Թ� a������������ԣ��a����b���� |
| �� | ���������Թ��зֱ����10.0 mLˮ���������۲����� | / |
| �� | �ٷֱ������Թ��еμ�2�η�̪��Һ���۲����� | ��Һ����죬��ɫ������Թ��� a���a����b������ |
| �� | ���ֱ�������Һ�еμ��������ᣮ | ��ɫ��ȥ��������ɫ��������������������������a ��b���������������=���� |
| �� | ���ȴ��Թ�һ��ʱ�䣮��ע������մ����ˮ����ͭ��ĩ�� | / |

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 13��8��29 | B�� | 39��24��13 | C�� | 22��11��14 | D�� | 26��16��57 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ������õķ�������������ʹҩ���������·����ϳɣ�
������õķ�������������ʹҩ���������·����ϳɣ�

 ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
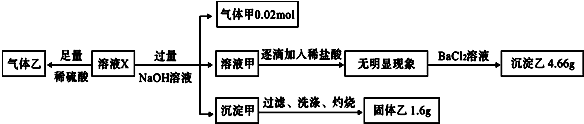
| A�� | ����ס�������һ��Ϊ������ | |
| B�� | CO32-��Al3+��K+һ�������� | |
| C�� | SO42-��NH4+һ�����ڣ�NO3-��Cl-���ܲ����� | |
| D�� | ������Fe3+����һ������Cl- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� |  ���� | B�� |  ���� | ||
| C�� |  ��ȡ | D�� |  �����ЧӦ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Ba��OH��2��Һ�еμ�NaHSO4��Һ�����ԣ�Ba2++2OH-+2H++SO${\;}_{4}^{2-}$�TBaSO4��+2H2O | |
| B�� | ���Ȼ�����Һ�ͷ�ˮ��Ӧ��ȡ�����������壺Fe3++3H2O����ˮ���TFe��OH��3��+3H+ | |
| C�� | ����ˮ��Ӧ��Na+2H2O=Na++2OH-+H2�� | |
| D�� | ����ʯ��ˮ��ϡ���ᷴӦ��Ca��OH��2+2H+=Ca2++2H20 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
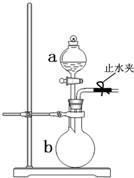 ��ͼ��ʾװ����ʵ���ҳ��õ�������ȡװ�ã���ͼ�ش��������⣺
��ͼ��ʾװ����ʵ���ҳ��õ�������ȡװ�ã���ͼ�ش��������⣺�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com