
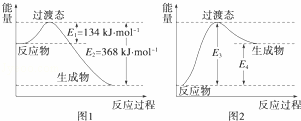
过渡态理论认为:化学反应并不是通过简单的碰撞就能完成的,而是从反应物到生成物的过程中经过一个高能量的过渡态.如图1是1mol NO2与1mol CO恰好反应生成CO2和NO过程中的能量变化示意图.
(1)试写出NO2和CO反应的热化学方程式: NO2(g)+CO(g)═NO(g)+CO2(g)△H=﹣234kJ•mol﹣1 .该反应的活化能是 134 kJ•mol﹣1.
(2)在密闭容器中进行的上述反应是可逆反应,则其逆反应的热化学方程式为 NO(g)+CO2(g)═NO2(g)+CO(g)△H=+234kJ•mol﹣1 ,该反应的活化能为 368 kJ•mol﹣1.
(3)图2是某学生模仿图1画出的NO(g)+CO2(g)═NO2(g)+CO(g)的能量变化示意图.则图中E3= 368 kJ•mol﹣1,E4= 234 kJ•mol﹣1.
| 反应热和焓变;热化学方程式.. | |
| 专题: | 化学反应中的能量变化. |
| 分析: | (1)根据能量变化图,反应热等于正反应的活化能减去逆反应的活化能; 图中E1是活化能,即该反应的活化能为134kJ•mol﹣1; (2)可逆反应的逆反应的反应热应该与正反应的数值相等,但符号相反,图中E2是逆反应的活化能; (3)E3即为逆反应的活化能,E4是反应物与生成物的能量之差,即为反应热. |
| 解答: | 解:(1)该反应的焓变△H=E1﹣E2=134KJ/mol﹣368KJ/mol=﹣234KJ/mol,所以热化学方程式为:NO2(g)+CO(g)═NO(g)+CO2(g) △H=﹣234kJ•mol﹣1,图中E1是活化能,即该反应的活化能为134kJ•mol﹣1; 故答案为:NO2(g)+CO(g)═NO(g)+CO2(g)△H=﹣234kJ•mol﹣1;134kJ•mol﹣1; (2)可逆反应的逆反应的反应热应该与正反应的数值相等,但符号相反,故热化学方程式为:NO(g)+CO2(g)═NO2(g)+CO(g) △H=+234kJ•mol﹣1,图中E2是逆反应的活化能,即逆反应放热活化能为:368KJ/mol; 故答案为:NO(g)+CO2(g)═NO2(g)+CO(g)△H=+234kJ•mol﹣1;368; (3)E3即为逆反应的活化能,即为368KJ/mol,E4是该反应的反应热,即为234KJ/mol,故答案为:368;234. |
| 点评: | 本题考查了热化学方程式的书写,要注意,正逆反应的反应热数值相等,符号相反. |


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
下列叙述正确的是
A.向含有CaCO3沉淀的水中通入CO2至沉淀恰好溶解,再向溶液中加入NaHCO3饱和溶液,又有CaCO3沉淀生成
B.向Na2 CO3溶液中逐滴加入含等物质的量HCl的稀盐酸,生成的CO2与原Na2 CO3的物质的量之比为1:2
C.等质量的Na HCO3和Na2 CO3分别与足量盐酸反应,在同温同压下,生成的CO2体积相同
D.向Na2 CO3饱和溶液中通入CO2,有Na HCO3结晶析出
查看答案和解析>>
科目:高中化学 来源: 题型:
美托洛尔是一种治疗高血压的药物的中间体,可以通过以下方法合成:

请回答下列问题:
(1)美托洛尔中的含氧官能团为 和 (填名称)。
(2)反应③中加入的试剂X的分子式为C2H5OCl,X的结构简式为 。
(3)在上述①②③三步反应中,属于取代反应的是 (填序号)。
(4)B的一种同分异构体满足下列条件:
Ⅰ.能发生银镜反应 Ⅱ.能与FeCl3溶液发生显色反应
Ⅲ.分子中有4种不同化学环境的氢,且1 mol该物质与金属钠反应产生 1 mol H2。
写出一种该同分异构体的结构简式: 。
(5)根据已有知识并结合题目所给相关信息,写出以CH3OH和 为原料制备
为原料制备 的合成路线流程图(无机试剂任用)。合成路线流程图示例如下:
的合成路线流程图(无机试剂任用)。合成路线流程图示例如下:

查看答案和解析>>
科目:高中化学 来源: 题型:
下列生产或实验事实引出的相应结论不正确的是( )
| 选项 | 事实 | 结论 |
| A | 其他条件相同,Na2S2O3溶液和H2SO4溶液反应,升高溶液的温度,析出硫沉淀所需时间缩短 | 当其他条件不变时,升高反应温度,化学反应速率加快 |
| B | 工业制硫酸中,在SO3的吸收阶段,吸收塔里要装填瓷环 | 增大气液接触面积,使SO3的吸收速率增大 |
| C | 在容积可变的密闭容器中发生反应:2NH3(g)⇌N2H4(l)+H2(g),把容积的体积缩小一半 | 正反应速率加快,逆反应速率减慢 |
| D | A、B两支试管中分别加入等体积5%的H2O2溶液,在B试管中加入2~3滴FeCl3溶液,B试管中产生气泡快 | 当其他条件不变时,催化剂可以改变化学反应速率 |
|
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:
将一定量的氨基甲酸铵固体置于某容积恒定的真空容器中,发生反应:H2NCOONH4(s)⇌2NH3(g)+CO2(g)在不同温度下,该反应平衡状态部分数据见表.下列说法正确的是( )
| 温度 | 平衡浓度/(mol L﹣1) | |
| c(NH3) | c(CO2) | |
| T1 | 0.1 | |
| T2 | 0.1 |
|
| A. | 若T2>T1,则该反应的△H<0 |
|
| B. | 向容器中充入N2,H2NCOONH4质量增加 |
|
| C. | NH3体积分数不变时,说明该反应达到平衡 |
|
| D. | T1、T2时,H2NCOONH4转化的△n(T2)=2△n(T1) |
查看答案和解析>>
科目:高中化学 来源: 题型:
化学与环境、材料、信息、能关系密切,下列说法正确的是
A.半导体行业中有一句话:“从沙滩到用户”,计算机芯片的材料是二氧化硅
B.绿色化学的核心是利用化学原理治理环境污染
C.将煤气化或液化,获得清洁燃料
D.PM2.5是指大气中直径接近于2.5×10-6 m的颗粒物,也称细颗粒物,这些细颗粒物分散在空气中形成混合物具有丁达尔效应
查看答案和解析>>
科目:高中化学 来源: 题型:
甲、乙、丙、丁均为中学化学中常见的单质或化合物,它们之间的转化关系如下图所示(部分产物已略去),下列各组物质中不能按图示关系转化的是
| 选项 | 物质转化关系 | 甲 | 乙 | 丙 | 丁 |
| A |
| NaOH | NaHCO3 | Na2CO3 | CO2 |
| B | AlCl3 | NaAlO2 | Al(OH)3 | NaOH | |
| C | Fe | Fe(NO3)3 | Fe(NO3)2 | HNO3 | |
| D | C | CO | CO2 | O2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列各化学反应的离子方程式中,有错误的是( )
A.铝与氢氧化钠反应:2Al+2OH-+2H2O=2AlO2-+3 H2↑
B.氧化铝溶于氢氧化钠溶液:Al2O3+2OH-=2AlO2-+H2O
C.碘化亚铁溶液中滴入足量溴水:2Fe2++2I-+2Br2=I2+2Fe3++4Br-
D.碳酸氢镁溶液中加过量澄清石灰水
Mg2++2HCO3-+2Ca2++4OH-=2CaCO3↓+2H2O+Mg(OH)2↓
查看答案和解析>>
科目:高中化学 来源: 题型:
某溶液中可能含有OH—、CO32—、AlO2—、SiO32—、SO42—、HCO3—、Na+、Fe3+、Mg2+、
Al3+ 等离子。当向该溶液中逐滴加入一定物质的量浓度的盐酸溶液时,发现生成沉淀的物质的量随盐酸溶液的体积变化的图像如下图所示。下列说法正确的是
A.原溶液中一定含有的阴离子是:OH—、SiO32—、AlO2—、CO32—
B.反应最后形成的溶液中的溶质为NaCl
C.原溶液中一定含有Na2SO4
D.原溶液中含有CO32- 与AlO2- 的物质的量之比为1∶2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com