
| A.c(M+)>c(OH-)>c(A-)>c(H+) | B.c(M+)> c(A-) > c(H+)> c(OH-) |
| C.c(M+)> c(A-) > c(OH-) >c(H+) | D.c(M+)> c(H+) >c(A-)> c(OH-) |
科目:高中化学 来源:不详 题型:填空题
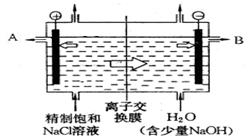
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.“E85”是由两种物质组成的一种燃料,属新能源 |
| B.推广使用乙醇汽油是为了减少温室气体排放 |
| C.等质量的“E85”和汽油充分燃烧后放出的能量相等 |
| D.乙醇属可再生性能源 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.弱碱 | B.一元强碱 | C.多元强碱 | D.任何强碱 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
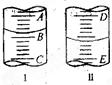
| A.是amL | B.是(25-a)mL |
| C.一定大于amL | D.一定大于(25-a)mL |
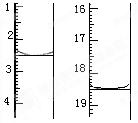
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.强电解质都是离子化合物,而弱电解质都是共价化合物 |
| B.中和PH值相等、体积相等的盐酸和醋酸,盐酸所消耗的氢氧化钠少 |
| C.将氢氧化钠和氨水溶液各稀释一倍,两者的OH-浓度均减小到原来的1/2 |
| D.常温下,PH为12的溶液一定是碱溶液 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:计算题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com