
| A. | 升高温度可使该反应的逆反应速率降低 | |
| B. | 使用高效催化剂只能提高正反应速率 | |
| C. | 反应达到平衡后,NO的反应速率为零 | |
| D. | 单位时间内消耗CO和CO2的物质的量相等时,反应达到平衡 |
分析 A.升高温度正逆反应速率都增大;
B.催化剂增大正逆反应速率;
C.反应达到平衡后,正逆反应速率相等,且不变;
D.达到平衡状态,单位时间内消耗CO和CO2的物质的量相等.
解答 解:A.无论放热反应还是吸热反应,升高温度正逆反应速率都增大,故A错误;
B.催化剂改变活化能,催化剂增大正逆反应速率,所以使用高效催化剂可有效提高正逆反应速率,故B错误;
C.反应达到平衡后,正逆反应速率相等,且不变,所以反应达到平衡后,NO的反应速率保持恒定,而不等于0,故C错误;
D.达到平衡状态,单位时间内消耗CO和CO2的物质的量相等,即正逆反应速率,所以能据此判断平衡状态,故D正确;
故选D.
点评 本题考查化学反应速率影响因素、化学平衡状态的判断等知识点,知道只有反应前后改变的物理量才能作为平衡状态的判断依据,题目难度不大.


 培优口算题卡系列答案
培优口算题卡系列答案 开心口算题卡系列答案
开心口算题卡系列答案 口算题卡河北少年儿童出版社系列答案
口算题卡河北少年儿童出版社系列答案科目:高中化学 来源: 题型:选择题
| A. | 最常见的氢化物的沸点:Y>X>W>Z | |
| B. | 简单离子半径:W>X>Y>Z | |
| C. | Y与Z能形成化学键类型完全相同的两种化合物 | |
| D. | Z与W形成的常见化合物溶于水后,水的电离程度变小 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 44 g由CO2和N20组成的混合气体中的氧原子数为2NA | |
| B. | 1 mol由异丁烷和正丁烷组成的混合物中含有的共价键数目为13NA | |
| C. | 2 mol SO2与2 molO2充分反应生成的SO2分子数为NA | |
| D. | 100 mL 12 mol•L-1浓盐酸与足量MnO2反应,转移的电子数为0.6NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Fe3++S2-=Fe2++S | B. | Fe3++Fe=2Fe2+ | ||
| C. | Fe2++Cl2=Fe3++2Cl- | D. | 2Fe3++2I-=2Fe2++I2 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
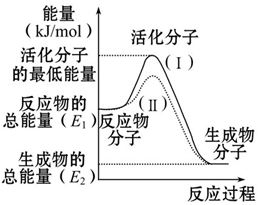 请认真观察如图,然后回答问题:
请认真观察如图,然后回答问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
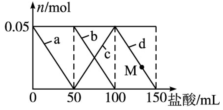 向100mL含Na2CO3、NaAlO2的混合溶液中逐滴加入150mL 1mol•L-1HCl溶液,测得溶液中的某几种离子物质的量的变化如图所示,则下列说法正确的是( )
向100mL含Na2CO3、NaAlO2的混合溶液中逐滴加入150mL 1mol•L-1HCl溶液,测得溶液中的某几种离子物质的量的变化如图所示,则下列说法正确的是( )| A. | a曲线表示的离子方程式为:AlO2-+H++H2O═Al(OH)3↓ | |
| B. | b曲线表示碳酸钠和盐酸反应,d曲线表示氢氧化铝的溶解 | |
| C. | M点时,溶液中沉淀的质量小于3.9 g | |
| D. | 原混合溶液中的Na2CO3溶液的浓度为1 mol•L-1 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com