
【题目】下列有关说法正确的是( )。
A.同浓度、同体积的强酸与强碱溶液混合后,溶液的pH一定等于7
B.0.1molAgCl和0.1AgBr混合后加入水中,所得溶液![]()
C.向0.1mol/LNa2SO3溶液中通SO2气体至溶液pH=7:![]()
D.0.1mol/LNH4Cl溶液与0.1mol/L氨水等体积混合pH>7:c(NH3H2O)>c(NH4+)>c(Cl-)>c(OH-)
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】已知25 ℃时,CaSO4在水中的沉淀溶解平衡曲线如图所示,向100 mL该条件下的CaSO4饱和溶液中加入400 mL 0.01 mol·L-1Na2SO4溶液,下列叙述正确的是
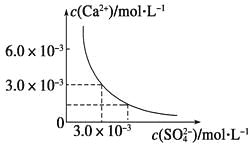
A.溶液中析出CaSO4固体沉淀,最终溶液中c(SO42-)比原来的大
B.溶液中无沉淀析出,溶液中c(Ca2+)、c(SO42-)都变小
C.溶液中析出CaSO4固体沉淀,溶液中c(Ca2+)、c(SO42-)都变小
D.溶液中无沉淀析出,但最终溶液中c(SO42-)比原来的大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】中国传统文化对人类文明贡献巨大,下列古代文献中充分记载了古代化学研究成果,对其说明不合理的是
选项 | 古代文献 | 说明 |
A. |
| 陶是一种传统硅酸盐材料 |
B. | 李白诗句“日照香炉生紫烟,遥看瀑布挂前川” | 诗中未涉及化学变化 |
C. |
| 文中涉及的操作方法有溶解、萃取、过滤 |
D. |
| 冰的能量低于水,冰转化为水属于吸热反应 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某课外小组设计的实验室制取乙酸乙酯的装置如图所示,A中放有浓硫酸,B中放有乙醇、无水醋酸,D中放有饱和碳酸钠溶液。

已知:①无水氯化钙可与乙醇形成难溶于水的CaCl2·6C2H5OH;无水硫酸钠可吸水作干燥剂。
②有关有机物的沸点见下表:
试剂 | 乙醚 | 乙醇 | 乙酸 | 乙酸乙酯 |
沸点(℃) | 34.7 | 78.5 | 118 | 77.1 |
请回答:
(1)图中仪器B的名称为________________;若产物水分子中氧原子为18O,写出能表示18O位置的乙酸乙酯制取的化学方程式____________________________________________。
(2)球形干燥管C的作用是__________________________,若反应前D中加入几滴酚酞,溶液呈红色,反应结束后D中的现象是____________________________________。
(3)从D中分离出的乙酸乙酯中常含有一定量的乙醇、乙醚和水,应先加入无水氯化钙,分离出____________;再加入(此空从下列选项中选择)___________;然后进行蒸馏,收集77℃左右的馏分,以得到较纯净的乙酸乙酯。
A.五氧化二磷 B.碱石灰 C.无水硫酸钠 D.生石灰
(4)从绿色化学的角度分析,使用浓硫酸制乙酸乙酯不足之处主要有________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业产生的废气COx、NOx、SOx对环境有害,若能合理的利用吸收,可以减少污染,变废为宝。
(1)已知甲烷的燃烧热为890 kJ/mol;1 mol水蒸气变成液态水放热44 kJ;N2与O2反应生成NO的过程如下:
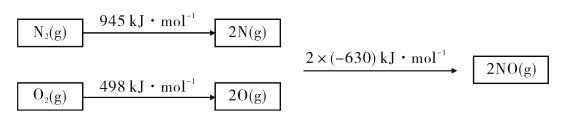
则CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g) △H=_______.
(2)汽车尾气中含有CO和NO,某研究小组利用反应:2CO(g)+2NO(g) ![]() N2 (g)+2CO2 (g)实现气体的无害化排放。T1℃时,在恒容的密闭容器中通入一定量的CO和NO,能自发进行上述反应,测得不同时间的NO和CO的浓度如下表:
N2 (g)+2CO2 (g)实现气体的无害化排放。T1℃时,在恒容的密闭容器中通入一定量的CO和NO,能自发进行上述反应,测得不同时间的NO和CO的浓度如下表:
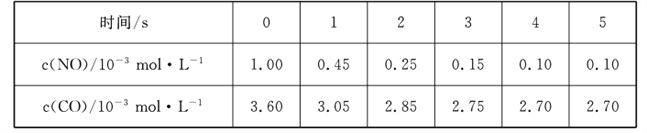
①0~2 s内用N2表示的化学反应速率为____,该温度下,反应的平衡常数K1_____。
②若该反应在绝热恒容条件下进行,则反应达到平衡后体系的温度为T2℃,此时的化学平衡常数为K2,则K1____K2(填“>”、“<”或“=”),原因是________
(3)向甲、乙两个容积均为1 L的恒温恒容的密闭容器中,分别充入一定量的SO2和O2(其中,甲充入2 mol SO2、1 mol O2,乙充入1 mol SO2、0.5 mol O2),发生反应:2SO2(g)+O2 (g) ![]() 2SO3 (g) △H= -197. 74 kJ/mol ,一段时间后达到平衡,测得两容器中c(SO2)(mol/L)随时间t(min)的变化关系如右图所示。下列说法正确的是______
2SO3 (g) △H= -197. 74 kJ/mol ,一段时间后达到平衡,测得两容器中c(SO2)(mol/L)随时间t(min)的变化关系如右图所示。下列说法正确的是______
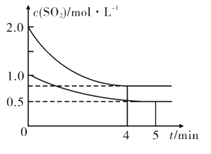
A.放出的热量Q:Q(甲)>2Q(乙)
B.体系总压强p:p(甲)>2p(乙)
C.甲容器达到化学平衡时,其化学平衡常数为4
D.保持其他条件不变,若起始时向乙中充入0.4 mol SO2、0.2mol O2、0.4 molSO3,则此时v(正>v(逆)
(4)在强酸性的电解质水溶液中,惰性材料做电极,电解CO2可得到多种燃料,其原理如右图所示。
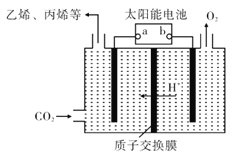
①该工艺中能量转化方式主要有____。
②电解时,生成乙烯的电极反应式是____。
(5)CO2在自然界循环时可与CaC03反应,Ca-CO3是一种难溶物质,其Ksp=2.8×10-9。CaCl2溶液与Na2 CO3溶液混合可形成CaCO3沉淀,现将等体积的CaCl2溶液与Na2 CO3溶液混合,若Na2 C03溶液的浓度为2×10-4 mol/L,则生成沉淀所需CaCl2溶液的最小浓度为_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室用如图所示的装置制取乙酸乙酯,下列说法中不正确的是( )
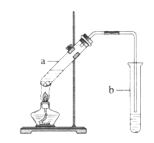
A.及时将乙酸乙酯蒸出,平衡向生成乙酸乙酯的方向移动
B.向试管a中先加入浓硫酸,然后边摇动试管边慢慢加入乙醇,再加冰醋酸
C.试管b中导气管下端不能浸入液面的目的是防止实验过程中产生倒吸现象
D.反应结束后用分液的方法分离试管b中的混合液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】多巴胺是一种神经传导物质,会传递兴奋及开心的信息。其部分合成路线如下,下列说法正确的是
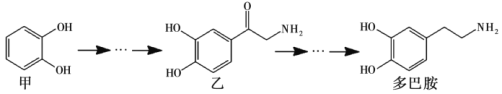
A. 甲在苯环上的溴代产物有2种
B. lmol乙与H2发生加成,最多消耗3molH2
C. 多巴胺分子中所有碳原子可能处在同一平面
D. 甲、乙、多巴胺3种物质均属于芳香烃
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】尼泊金酯是国际上公认的广谱性高效防腐剂,被广泛应用于食品、医药和化妆品的防腐等领域。我国国标规定,尼泊金酯中的乙酯、丙酯可用于食品。尼泊金丙酯(其相对分子质量约为180)在酸性条件下水解可生成两种有机物A和B。A的红外光谱表征到了羧基、羟基和苯环的存在,核磁共振氢谱表明其有4种不同化学环境的氢原子,且峰面积比为1:2:2:1。
(1)尼泊金丙酯中的含氧官能团的名称为________。
(2)为确定B的结构,可采用下列方法中的____________(填序号)。
a. 质谱法
b. 核磁共振氢谱法
c. 检验能否与NaHCO3溶液反应生成CO2
d. 检验能否发生氧化反应,并最终被氧化成羧酸
(3)写出A与足量NaOH溶液反应的化学方程式:________。
(4)尼泊金乙酯的同分异构体中,满足下列条件的共有___________种。
a. 分子中苯环上有两个对位取代基 b. 属于酯类 c. 可与浓溴水发生取代反应
写出这些同分异构体中,不含甲基的有机物的结构简式___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某酸式盐NaHY的水溶液显碱性,下列叙述正确的是![]()
![]()
A.![]() 的电离方程式:
的电离方程式:![]()
B.![]() 的水解方程式:
的水解方程式:![]()
C.该酸式盐溶液中离子浓度关系:![]()
D.该酸式盐溶液中离子浓度关系:![]()
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com