
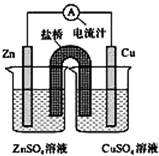
 如图为一原电池的装置示意图,下列说法不正确的是( )
如图为一原电池的装置示意图,下列说法不正确的是( )| A、原电池工作时的总反应为:Zn+Cu2+=Zn2++Cu |
| B、原电池工作时,电流由铜极流经电流计流向锌极 |
| C、原电池工作时,盐桥中K+移向CuSO4溶液 |
| D、如果将Cu电极与Zn电极互换,电流计指针反向偏转 |


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 族 周期 |
IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
| 2 | H | A | ||||||
| 3 | B | C | D | E | ||||
| 4 | F | G |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、减压 | B、加压 |
| C、升温 | D、使用催化剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、KHCO3溶液中混有K2CO3(CO2) |
| B、NaOH固体中混有Na2O2(H2O) |
| C、Na2CO3溶液中混有NaHCO3(CaCl2) |
| D、KNO3固体中混有KHCO3(HNO3) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、HMnO4 |
| B、H2SeO3 |
| C、H3BO3 |
| D、H3PO4 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、负极,发生氧化反应 |
| B、正极,发生氧化反应 |
| C、负极,发生还原反应 |
| D、正极,发生还原反应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com