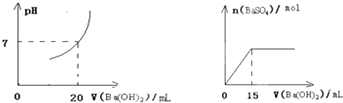捕碳技术(主要指捕获CO
2)在降低温室气体排放中具有重要的作用,目前NH
3和(NH4)
2CO
3已经被用作工业捕碳剂.
(1)已知CO
2与NH
3 经过两步反应可生成尿素,两步反应的能量变化示意图如图:

则NH
3(g) 与CO
2(g) 反应生成尿素的热化学方程式为
.
(2)已知CO
2与(NH
4)
2CO
3反应如下:(NH
4)
2CO
3(aq)+H
2O(l)+CO
2(g)?2NH
4HCO
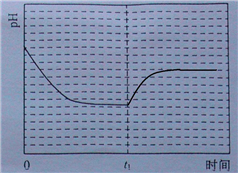
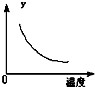
3(aq)△H<0,该反应在温度为T
1时,溶液的pH随时间变化的趋势曲线如图1所示.当时间达到t
1时,将该反应体系温度迅速上升到T
2,并维持该温度,在t
2达到新的平衡.请在图1中画出t
1时刻后溶液的pH变化总趋势曲线.在(NH
4)
2CO
3初始浓度不变的情况下,提高CO
2吸收量的措施有:
,
(写出2个)
(3)工业上也可用CO
2与H
2反应生成甲醇,其反应为:CO
2(g)+3H
2(g)?CH
3OH(g)+H
2O(g)△H=-49.0kJ/mol.在T℃下,将1mol CO
2和2mol H
2充入0.5L恒容密闭容器中,测得H
2的物质的量随时间的变化情况如图2所示.
①按曲线计算反应从0到4min时,v(H
2)=
.
②在T℃时,若仅改变某一外界条件时,测得H
2的物质的量随时间的变化情况如图2曲线Ⅱ所示,则改变的外界条件为
.反应按曲线Ⅱ进行,计算达到平衡时容器中c(CO
2)=
.
③判断该反应达到平衡的依据为
(填正确选项的字母)
A.混合气体的平均相对分子质量不随时间改变
B.3v(H
2)正=v(CH
3OH)逆
C.混合气体的压强不随时间改变
D.单位时间内生成CH
3OH和H
2O的物质的量相同




 ;
;  ;降低温度;增大CO2浓度;
;降低温度;增大CO2浓度;

 名牌学校分层周周测系列答案
名牌学校分层周周测系列答案 黄冈海淀全程培优测试卷系列答案
黄冈海淀全程培优测试卷系列答案


 (1)t℃时水的离子积为1×10-13,则该温度(选填大于、小于或等于)
(1)t℃时水的离子积为1×10-13,则该温度(选填大于、小于或等于)