
| A、Na2O2与H2O反应制备O2:Na2O2+H2O═2Na++2OH-+O2↑ |
| B、用FeCl3溶液腐蚀铜线路板:Cu+2Fe3+═Cu2++2Fe2+ |
| C、将氯气溶于水制备次氯酸:Cl2+H2O═2H++Cl-+ClO- |
| D、用浓盐酸酸化的KMnO4与H2O2反应,证明H2O2具有还原性:2MnO4-+6H++5H2O2═2Mn2++5O2↑+8H2O |


科目:高中化学 来源: 题型:
| A、生成n mol的A2,同时生成 n mol的AB |
| B、密闭容器内总压强不随时间变化 |
| C、生成2n mol的AB,同时生成n mol的B2 |
| D、生成n mol的A2,同时生成的n molB2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
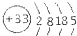 ,做出如下推理,其中与事实不符的是( )
,做出如下推理,其中与事实不符的是( )| A、砷元素位于元素周期的第四周期、第VA族 |
| B、砷原子不如溴原子的得电子能力强 |
| C、砷酸酸性比磷酸酸性强 |
| D、在相同条件砷元素的氢化物的稳定性弱于氨气 |
查看答案和解析>>
科目:高中化学 来源: 题型:
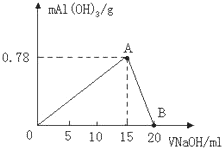 向20mL某物质的量浓度的AlCl3溶液中滴入2mol/LNaOH溶液时,得到的Al(OH)3沉淀质量与所加NaOH溶液体积(mL)的关系如图所示,试回答下列问题:
向20mL某物质的量浓度的AlCl3溶液中滴入2mol/LNaOH溶液时,得到的Al(OH)3沉淀质量与所加NaOH溶液体积(mL)的关系如图所示,试回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:
| A、向烧碱溶液中滴加石蕊试液,溶液呈蓝色,然后通CO2至颜色变红:CO2+H2O?H++HCO3- |
| B、向Fe(NO3)3溶液中加入过量的HI溶液:2Fe3++2I-═2Fe2++I2 |
| C、碳酸氢铵溶液中加足量石灰水:NH4++HCO3-+Ca2++2OH-═CaCO3↓+NH3?H2O+H2O |
| D、84消毒液和洁厕灵混合使用会产生有毒气体:Cl-+ClO-+2H+═Cl2↑+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、AlCl3溶液中滴加足量氨水:Al3++4OH-=AlO2-+2H2O |
| B、Fe(OH)3溶于氢碘酸:Fe(OH)3+3H+=Fe3++3H2O |
| C、向NaAlO2溶液中通入过量CO2制Al(OH)3:AlO2-+CO2+2H2O=Al(OH)3↓+HCO3- |
| D、钠和水反应:Na+2H2O=Na++2OH-+H2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:
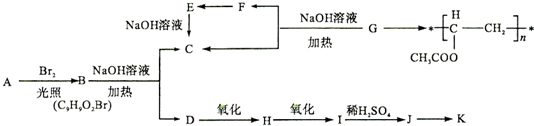
查看答案和解析>>
科目:高中化学 来源: 题型:
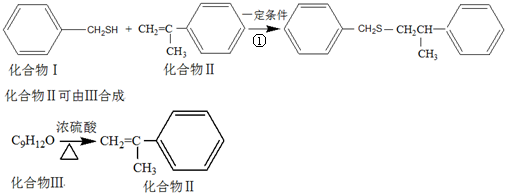
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com