
【题目】向50mLNa2SO4和Na2CO3的混合溶液中加入过量的BaCl2溶液,得到14.51g白色沉淀,向白色沉淀中加入过量的稀HNO3,充分反应后,沉淀减少到4.66g,并有气体产生。
(1)原混合溶液中Na2SO4和Na2CO3的物质的量浓度各是______。
(2)产生的气体在标准状况下的体积是______。
【答案】0.4mol/L;1mol/L1.12L
【解析】
(1)14.51克白色沉淀是BaCO3和BaSO4混合物,BaSO4不溶于水与硝酸,BaCO3溶于硝酸,故白色沉淀中加入过量的稀HNO3,充分反应后,沉淀减少到4.66g为BaSO4的质量,可得BaCO3的质量为14.51g-4.66g=9.85g,根据n=![]() 计算BaCO3和BaSO4的物质的量,Na2SO4的物质的量等同于BaSO4的物质的量,Na2CO3的物质的量等同于BaCO3的物质的量,再根据c=
计算BaCO3和BaSO4的物质的量,Na2SO4的物质的量等同于BaSO4的物质的量,Na2CO3的物质的量等同于BaCO3的物质的量,再根据c=![]() 计算原混和溶液中Na2CO3和Na2SO4的物质的量浓度;
计算原混和溶液中Na2CO3和Na2SO4的物质的量浓度;
(2)发生反应BaCO3+2HNO3═Ba(NO3)2+H2O+CO2↑,由方程式可知n(CO2)=n(BaCO3),再根据V=nVm计算CO2的体积。
(1)14.51克白色沉淀是BaCO3和BaSO4混合物,加入过量的稀HNO3,充分反应后,剩余沉淀4.66g为BaSO4,BaSO4的物质的量为![]() =0.02mol,由硫酸根守恒可知n(Na2SO4)=n(BaSO4)=0.02mol,所以Na2SO4物质的量的浓度为
=0.02mol,由硫酸根守恒可知n(Na2SO4)=n(BaSO4)=0.02mol,所以Na2SO4物质的量的浓度为![]() =0.4mol/L,
=0.4mol/L,
减少的沉淀质量为BaCO3,故BaCO3的质量为14.51g-4.66g=9.85g,物质的量为![]() =0.05mol,由碳酸根守恒可知n(Na2CO3)=n(BaCO3)=0.05mol,所以Na2CO3的物质的量浓度为
=0.05mol,由碳酸根守恒可知n(Na2CO3)=n(BaCO3)=0.05mol,所以Na2CO3的物质的量浓度为![]() =1mol/L,
=1mol/L,
因此,本题正确答案为:0.4mol/L、1mol/L;
(2)发生反应BaCO3+2HNO3═Ba(NO3)2+H2O+CO2↑,由方程式可知n(CO2)=n(BaCO3)=0.05mol,故生成的二氧化碳的体积为0.05mol×22.4L/mol=1.12L,
因此,本题正确答案为:1.12L。


科目:高中化学 来源: 题型:
【题目】CaCO3与稀盐酸反应生成CO2的量与反应时间的关系如图所示。下列结论不正确的是
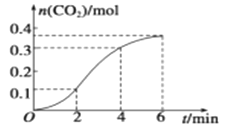
A. 反应在2~4 min内平均反应速率最大
B. 反应开始4 min内温度比浓度对反应速率的影响大
C. 4 min后,反应速率减小的主要原因是c(H+)减小
D. 反应在2~4 min内生成CO2的平均反应速率为v(CO2)=0.1 mol·L-1·min-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】亚硝酰氯(ClNO)常用作催化剂和合成洗涤剂,其沸点为-5.5℃,易水解。某学习小组在实验室中用下图所示装置制备ClNO。已知:HNO2既有氧化性又有还原性;AgNO2微于水,能溶于硝酸,AgNO2+HNO3=AgNO3+HNO2。
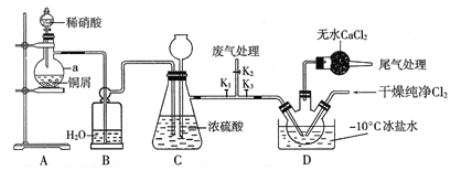
回答下列问题:
(1)仪器a的名称为_____________,装置B的作用是____________。
(2)装置C中长颈漏斗的作用是____________。
(3)实验开始时,先打开K1、K2,关闭K3,再打开分液漏斗活塞滴人适量稀硝酸,当观察到C中______时关闭K1、K2。向装置D三颈瓶中通人千燥纯净Cl2,当瓶中充满黄绿色气体时,再打开K1、K3,制备ClNO。
(4)装置D中干燥管的作用是__________________。
(5)实验过程中,若学习小组同学用酒精灯大火加热制取NO,对本实验造成的不利影响是____、________。
(6)ClNO与H2O反应生成HNO2和HCl。
①设计实验证明HNO2是弱酸________________。(仅提供的试剂:1mol/L盐酸、1mol/L HNO2、Na、NaNO2溶液、红色石蕊试纸、蓝色石蕊试纸)
②要验证ClNO与H2O反应后的溶液中存在Cl-和HNO2,合理的操作步骤及正确的顺序是_____(填序号)。
a.向烧杯中滴加过量KI淀粉溶液,溶液变蓝色
b.取1.0mL三颈瓶中产品于烧杯中,加入10.0mLH2O充分反应
c.向烧杯中滴加酸性KMnO4溶液,溶液紫色褪去
d.向烧杯中滴加足量AgNO3溶液,有白色沉淀生成,加入稀硝酸,搅拌,仍有白色沉淀
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列大小比较正确的是
A. 等体积、等物质的量浓度的NaCl(aq)离子总数小于NaClO(aq)中离子总数
B. 25 ℃时,pH=3的硫酸溶液中水的电离程度大于pH=11的氨水中水的电离程度
C. 0.1 mol·L-1(NH4)2CO3溶液中的c(NH![]() )大于0.1 mol·L-1的NH4Cl溶液中的c(NH
)大于0.1 mol·L-1的NH4Cl溶液中的c(NH![]() )的2倍
)的2倍
D. 常温下,将醋酸钠、盐酸两溶液混合后,溶液呈中性,溶液中c(Na+)大于c(Cl-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.需要加热方能发生的反应一定是吸热反应
B.放热反应在常温下一定很容易发生
C.反应是放热还是吸热,必须看反应物和生成物所具有的总能量的相对大小
D.化学反应只生成新物质,没有能量的变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】蒸馏水的制取:如图为实验室制取蒸馏水的装置示意图,根据图示回答下列问题。

(1)A仪器的名称是________,B仪器的名称是________。
(2)实验时A中除加入少量自来水外,还需加入少量________,其作用是___________。
(3)指出图中两处明显的错误,并改正:
①____________________;
②______________________。
(4)收集完蒸馏水后,是先撤酒精灯还是先关闭冷凝水?____________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值。下列说法正确的是
A. 标准状况下,22.4L.NO和11.2L O2反应,生成气体的分子数目为NA
B. 将CuO和Cu2S等质量混合,混合物中Cu2+数目为NA
C. 1L.pH=12的NaOH溶液中的OH-数目为0.01NA
D. 0.1molT218O所含电子数目为NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是 ( )
A. 25℃时 Cu(OH)2在水中的溶解度大于其在Cu(NO3)2溶液中的溶解度
B. 常温下,NaClO溶液显碱性的原因:ClO—+ H2O =" HClO" + OH—
C. 2NO(g) + 2CO(g) = N2(g) + 2CO2(g),在常温下能自发进行,则该反应的△H >0
D. 25℃时向水中加入少量NaOH后,由水电离出的c(H+)c(OH—)不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以2氯丙烷为主要原料制1,2丙二醇[CH3CH(OH)CH2OH]时,依次经过的反应类型为( )
A. 加成反应→消去反应→取代反应
B. 消去反应→加成反应→取代反应
C. 消去反应→取代反应→加成反应
D. 取代反应→加成反应→消去反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com