
【题目】下列所用材料不属于合金的是
A.家用的铝窗B.温度计用的水银
C.铸造用的黄铜D.建筑用的钢筋
科目:高中化学 来源: 题型:
【题目】某化学兴趣小组同学利用下图所示装置(夹持及加热装置已略去,装置气密性良好)探究SO2的性质(实验前已事先除去装置中的空气)。请回答下列问题:
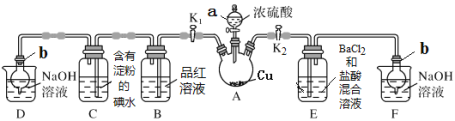
[查阅资料得知浓硫酸的沸点为338 ℃,酒精灯火焰的温度为400~500 ℃]
(1)仪器a的名称_________。
(2)装置D和F的作用是_________。
(3)加热时,装置A中反应的化学方程式为________。
(4)打开K1,关闭K2,加热装置A一段时间后,B中的现象是_____,当装置C中溶液由蓝色变为无色,由此推测所得无色溶液中的离子主要是H+、I- 和____;为了进一步实验证实了该过程中SO2已被氧化,该实验操作及现象是:_____。
(5)关闭K1,打开K2,用酒精灯加热装置A,观察到E中发生的现象是:有白色沉淀产生,白色沉淀的成分是_____,生成白色沉淀的原因可能是___(选填字母序号)。
a.SO2与BaCl2溶液反应生成了白色沉淀
b.BaCl2溶液与硫酸蒸气反应生成了白色沉淀
c.SO2溶于水生成的H2SO3被装置内的O2氧化生成H2SO4,再与BaCl2反应生成白色沉淀
(6)取A中产生的SO2气体通入足量双氧水中,然后加入足量BaCl2溶液,经过滤、洗涤、干燥得到4.66 g沉淀。据此推知SO2气体的体积为___mL(标准状况)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知反应:2X(g)+Y(g) ![]() 2Z(g)。某研究小组将4 mol X和2 mol Y置于一容积不变的密闭容器中,测定不同时间段内X的转化率,得到如下表数据:
2Z(g)。某研究小组将4 mol X和2 mol Y置于一容积不变的密闭容器中,测定不同时间段内X的转化率,得到如下表数据:
t(min) | 2 | 4.5 | 5 | 6 |
X转化率 | 30% | 40% | 70% | 70% |
根据以上信息作出的下列判断中正确的是( )
A. 随着反应的进行,混合气体的密度不断增大
B. 反应在5.5 min时,v正(X)=v逆(Z)
C. 6 min时,容器中剩余1.4 mol Y
D. 其他条件不变,将X的物质的量改为10 mol,则可得4 mol Z
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】[化学——选修5:有机化学基础]
诺氟沙星为喹诺酮类抗生素,其合成路线如下:
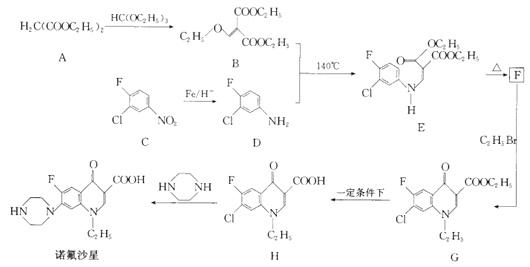
回答下列问题:
(1)化合物A的名称是____________。
(2)诺氟沙星分子中含氧官能团的名称为____________。
(3)C生成D,H生成诺氟沙星的反应类型分别是___________、___________。
(4)F的结构简式为_______________。
(5)G生成H的化学方程式为__________________。
(6)有机物X比B分子少一个CH2原子团,且含有酯基和![]() 结构其中核磁共振氢谱有三组峰,峰面积比为1:3:3的结构简式为__________(任写一种)
结构其中核磁共振氢谱有三组峰,峰面积比为1:3:3的结构简式为__________(任写一种)
(7)参照上述合成路线写出由有机物![]() 、B为有机原料合成
、B为有机原料合成 的路线图______________(无机试剂任选)。
的路线图______________(无机试剂任选)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在化学反应 3Cu+8HNO3→3Cu(NO3)2+2NO↑+4H2O 中,硝酸中被还原和未被还原的氮元素的质量比是
A. 3:1 B. 1:1 C. 1:2 D. 1:3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】石油化工生产中,利用裂解反应可以获得重要化工原料乙烯、丙烯。一定条件下,正丁烷裂解的主反应如下:
反应I C4H10(g)![]() CH4(g)+CH3CH-CH3(g) △H1;
CH4(g)+CH3CH-CH3(g) △H1;
反应Ⅱ C4H10(g)![]() C2H6(g)+CH2=CH2(g) △H2;
C2H6(g)+CH2=CH2(g) △H2;
回答下列问题:
(1)正丁烷、乙烷和乙烯的燃烧热分别为Q1kJ·mol-1、Q2kJ·mol-1、Q3kJ·mol-1,反应Ⅱ的△H2=______________。
(2)一定温度下,向容积为5L的密闭容器中通入正丁烷,反应时间(t)与容器内气体总压强(p)数据如下:
t/min | 0 | a | 2a | 3a | 4a |
p/MPa | 5 | 7.2 | 8.4 | 8.8 | 8.8 |
①该温度下,正丁烷的平衡转化率a=__________;反应速率可以用单位时间内分压的变化表示,即v=![]() ,前2a min内正丁烷的平均反应速率
,前2a min内正丁烷的平均反应速率![]() =__________MPa·min-1。
=__________MPa·min-1。
②若平衡时甲烷、乙烯的体积分数分别为![]() 、
、![]() ,则该温度下反应I的压力平衡常数Kp=_________MPa(用平衡分压代替平衡浓度计算,分压一总压×物质的量分数,保留三位有效数字)。
,则该温度下反应I的压力平衡常数Kp=_________MPa(用平衡分压代替平衡浓度计算,分压一总压×物质的量分数,保留三位有效数字)。
③若反应在恒温、恒压条件进行,平衡后反应容器的体积_________8.8L(填“>”“<”或“=”)。
④实际生产中发现高于640K后,乙烯和丙烯的产率随温度升高增加幅度减小,可能的原因是__________(任写1条)。
(3)一种丁烷燃料电池工作原理如图所示。

①A电极上发生的是反应_________(填“氧化“或“还原”)。
②写出B电极的电极反应式:______________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】通过传感器可以监测空气中甲醛的含量。一种燃料电池型甲醛气体传感器的原理如图所示,下列说法错误的是

A. a为电池的正极,发生还原反应
B. b极的电极反应为HCHO+H2O-4e-==CO2+4H+
C. 传感器工作过程中,电解质溶液中硫酸的浓度减小
D. 当电路中转移2×10-4 mol电子时,传感器内参加反应的HCHO为3.0 mg
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com