
【题目】常温下,HNO2的电离平衡常数为K=4.6×10-4(已知![]() =2.14),向20 mL 0.01 mol·L-1的HNO2溶液中逐滴加入相同浓度的NaOH溶液,测得混合液的pH随NaOH溶液体积的变化如图所示,下列判断正确的是( )
=2.14),向20 mL 0.01 mol·L-1的HNO2溶液中逐滴加入相同浓度的NaOH溶液,测得混合液的pH随NaOH溶液体积的变化如图所示,下列判断正确的是( )
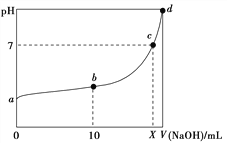
A. HNO2的电离方程式为HNO2===NO![]() +H+
+H+
B. a点H2O电离出的c(H+)=2.14×10-3 mol·L-1
C. b点溶液中离子浓度大小关系为c(NO![]() )>c(Na+)>c(H+)>c(OH-)
)>c(Na+)>c(H+)>c(OH-)
D. X值等于20
【答案】C
【解析】A.HNO2的电离平衡常数为K=4.6×10-4,亚硝酸为弱酸存在电离平衡,电离方程式为HNO2NO2-+H+,故A错误;B.由HNO2H++NO2-,K=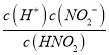 ≈
≈ ,4.6×10-4≈
,4.6×10-4≈![]() ,得到c(H+)=2.14×10-3mol/L,水电离出氢离子浓度远小于酸电离出氢离子,故B错误;C.b点溶液为HNO2、NaNO2混合溶液,且浓度比为1:1;由NO2-+H2OHNO2+OH-,HNO2H++NO2-,电离程度大于水解程度,可知溶液呈酸性,离子浓度大小为c(NO2-)>c(Na+)>c(H+)>c(OH-),故C正确;D.向20mL0.01molL-1的HNO2溶液中逐滴加入相同浓度的NaOH溶液,若恰好反应需要氢氧化钠溶液体积20ml,C点是溶液呈中性,溶质为HNO2、NaNO2混合溶液,X<20mL,故D错误;故选C。
,得到c(H+)=2.14×10-3mol/L,水电离出氢离子浓度远小于酸电离出氢离子,故B错误;C.b点溶液为HNO2、NaNO2混合溶液,且浓度比为1:1;由NO2-+H2OHNO2+OH-,HNO2H++NO2-,电离程度大于水解程度,可知溶液呈酸性,离子浓度大小为c(NO2-)>c(Na+)>c(H+)>c(OH-),故C正确;D.向20mL0.01molL-1的HNO2溶液中逐滴加入相同浓度的NaOH溶液,若恰好反应需要氢氧化钠溶液体积20ml,C点是溶液呈中性,溶质为HNO2、NaNO2混合溶液,X<20mL,故D错误;故选C。


 一线名师权威作业本系列答案
一线名师权威作业本系列答案科目:高中化学 来源: 题型:
【题目】在一定的温度和压强下,水成为“超临界状态”,此时水可将CO2等含碳化合物转化为有机物,这就是“水热反应”。生物质在地下高温高压条件下通过水热反应可生成石油、煤等矿物能源。下列说法错误的是
A. 二氧化碳与超临界水作用生成汽油的反应,属于放热反应
B. “水热反应”是一种复杂的化学变化
C. 火力发电厂可望利用废热,将二氧化碳转变为能源物质
D. 随着科技的进步,“水热反应”制取能源有望实现地球上碳资源的和谐循环
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物F(Bisphenol A dimethacrylate)是一种交联单体。合成F的一种路线如下:
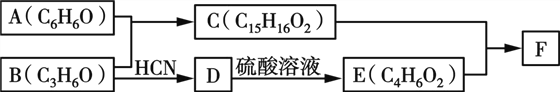
已知:
①![]() +HCN
+HCN![]()
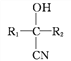
②B不能发生银镜反应。
③C能与FeCl3发生显色反应,核磁共振氢谱显示有4种不同化学环境的氢。
④E既能使溴水褪色又能使石蕊试液显红色。
⑤1 mol F最多可与4 mol NaOH反应。
回答下列问题:
(1)A与B反应的化学方程式为________________。
(2)B→D的反应类型为____,E的结构简式为________。
(3)F的结构简式为____________。
(4)C的同分异构体中含有萘环(![]() )结构,萘环上只有1个取代基且水解产物之一能与FeCl3溶液发生显色反应的同分异构体共有____种(不考虑立体异构),其中核磁共振氢谱有8组峰的是____________(写出其中一种的结构简式)。
)结构,萘环上只有1个取代基且水解产物之一能与FeCl3溶液发生显色反应的同分异构体共有____种(不考虑立体异构),其中核磁共振氢谱有8组峰的是____________(写出其中一种的结构简式)。
(5)A经如下步骤可合成环己烯甲酸:
A![]() G
G![]() H
H![]() I
I![]()
![]()
反应条件1为________;反应条件2为______;反应条件3所选择的试剂为____;I的结构简式为____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化工生产中常用MnS作沉淀剂除去工业废水中的Cu2+:Cu2+(aq)+MnS(s)![]() CuS(s)+Mn2+(aq)下列有关叙述中正确的是( )
CuS(s)+Mn2+(aq)下列有关叙述中正确的是( )
①MnS的Ksp大于CuS的Ksp ②达到平衡时c(Mn2+)=c(Cu2+) ③溶液中加入少量Na2S固体后,溶液中c(Cu2+)、c(Mn2+)保持不变 ④该反应平衡常数K=
A. ①④ B. ②③
C. ①②③ D. ②③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某KCl样品中含有少量K2CO3、K2SO4和不溶于水的杂质。为了提纯KCl,先将样品溶于适量水中,搅拌、过滤,再将滤液按下图所示步骤进行提纯(过滤操作已略去)。下列说法正确的是

A.起始滤液常温下pH=7 B.试剂Ⅰ为Ba(NO3)2溶液
C.上图过程须经2次过滤 D.步骤③目的是除去CO32-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、M、W为五种短周期元素,X、Y、Z是原子序数依次增大的同周期元素,且最外层电子数之和为15,X与Z可形成XZ2分子;Y与M形成的气态化合物在标准状况下的密度为0.76 g·L-1;W的质子数是X、Y、Z、M四种元素质子数之和的1/2。下列说法正确的是
A. 原子半径:W>Z>Y>X>M
B. 常见气态氢化物的稳定性:X<Y<Z
C. 1 mol WM溶于足量水中完全反应,共转移2 mol电子
D. 由X、Y、Z、M四种元素形成的化合物一定既有离子键,又有共价键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,Fe(OH)2和Cu(OH)2的饱和溶液中,金属阳离子的物质的量浓度的负对数[一lg c(M2+)]与溶液pH的变化关系如图所示,已知该温度下,Ksp[Cu(OH)2]2],下列说法正确的是 ( )

A. b线表示Fe(OH)2饱和溶液中的变化关系,且Ksp[Fe(OH)2]=10-15.1
B. 当Fe(OH)2和Cu(OH)2沉淀共存时,溶液中:C(Fe2+):C(Cu2+):1:104.6
C. 向X点对应的饱和溶液中加入少量NaOH,可转化为Y点对应的溶液
D. 除去CuSO4溶液中含有的少量Fe2+,可加入适量Cu0
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】近年来我国科技发展突飞猛进。下列设备工作时主要由化学能转化为电能的是
A.海上风力发电
B.“深海勇士”号潜水器的新型锂电池
C.北斗导航卫星的太阳能电池板
D.“长征5号”火箭使用的煤油液氧发动机
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D四种物质均易溶于水,分别按下列条件配成溶液,其中物质的量浓度最大的是
A. 0.1 moL D物质溶于100 mL 2.5 mol·L-1的D溶液中
B. 9.2 g B物质(式量为46)溶于水配成100 mL溶液
C. 1.806×1023个C的分子溶于水配成100 mL溶液
D. 10 mL 5mol·L-1的A溶液加水配制成100 mL溶液
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com