
【题目】假如你是一位企业家,在开发海水资源的众多项目中,选择了海水提镁,在前期考察过程中你将遇到许多问题,请根据背景材料的提示,按要求回答相关问题:
材料1:下图为海水中各元素含量情况(mg/L)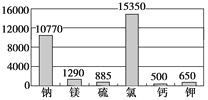
材料2:部分化学试剂的市场价格
试剂 | 氢氧化钾 | 氢氧化钠 | 氢氧化钙 | 氧化钙 |
价格(元/吨) | 5238.0 | 2300.00 | 1200.00 | 700.00 |
请回答下列问题:
(1)在海水提镁的过程中要实现对镁离子的富集、分离,有以下三个方案:
方案一:直接往海水中加入沉淀剂;
方案二:加热蒸发海水后再加入沉淀剂;
方案三:在晒盐后的卤水中加入沉淀剂。
你认为方案最合理。
不选方案的理由是。
不选方案的理由是。
(2)应该选择试剂作为镁离子的沉淀剂。不考虑其他费用,沉淀相同量的镁离子所用氢氧化钠和氧化钙的价格比为。
(3)为了节省成本,你可考虑以海边上的贝壳为原料,试简述其理由:?
 中考解读考点精练系列答案
中考解读考点精练系列答案 各地期末复习特训卷系列答案
各地期末复习特训卷系列答案 小博士期末闯关100分系列答案
小博士期末闯关100分系列答案科目:高中化学 来源: 题型:
【题目】聚四氟乙烯的耐热性和化学稳定性都超过了其他塑料,号称“塑料王”,在工业上有广泛的用途,其合成途径如下图所示: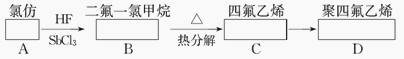
(1)在方框中填入合适的有机物的结构简式。
(2)写出下列反应化学方程式:B→C、C→D。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于能量变化的说法正确的是
A. 冰融化成水放出热量B. 生成物的总能量一定低于反应物的总能量
C. 金属与酸反应吸收能量D. 化学键的断裂和形成是化学反应中能量变化的主要原因
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图,缓慢通入O2 , 用水吸收NO2(假设每次通入的O2能完全反应).下列说法正确的是( ) 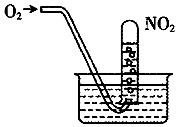
A.当试管内溶液的pH值不再变化,说明NO2全部转化为HNO3
B.当试管气体不是红棕色时,说明NO2全部转化为HNO3
C.水槽内的水改为稀盐酸,有利于吸收NO2
D.水槽内的水改为稀NaOH溶液,有利于吸收NO2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某班同学用如下实验探究Na2CO3、NaHCO3的性质.回答下列问题:
(1)甲组同学分别取1.0g Na2CO3、NaHCO3固体,各滴加几滴水,发现盛Na2CO3的试管温度上升,而盛NaHCO3的试管温度下降;原因是 .
(2)乙组同学分别取0.1mol/L Na2CO3、0.1mol/LNaHCO3的溶液,用0.1mol/LHCl溶液滴定,pH变化与盐酸体积的关系如图所示: 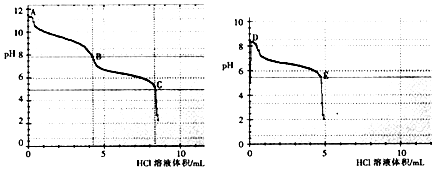
①碳酸钠与盐酸反应pH有两次突变,达到两次反应终点,分别是(填A、B、C、D或E).
②B点的主要溶质是(用化学式表示).
③B点(填“大于”或“小于”) D点的pH,主要原因是 .
(3)丙组同学预测NaHCO3有酸性,向其溶液加入镁粉,发现有气泡和沉淀生成,写出化学方程式: .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应既表现硝酸的酸性,又显示硝酸的氧化性的是
A. CuO+2HNO3=Cu(NO3)2+H2O B. FeO+4HNO3=Fe(NO3)3+2H2O+NO2↑
C. C+4HNO3=CO2↑+2H2O+4NO2↑ D. NH3+HNO3=NH4NO3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在两个密闭容器中,分别充有质量相同的甲、乙两种气体,若两容器的温度和压强均相同,且甲的密度大于乙的密度,则下列说法正确的是( )
A.甲的分子数比乙的分子数多
B.甲的摩尔体积比乙的摩尔体积小
C.甲的相对分子质量比乙的相对分子质量小
D.甲的物质的量比乙的物质的量少
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com