
| A. | MgCl2(熔融) $\frac{\underline{\;电解\;}}{\;}$ Mg+Cl2↑ | B. | Al2O3+3C $\frac{\underline{\;2125℃\;}}{\;}$2Al+3CO↑ | ||
| C. | Fe2O3+3CO $\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2 | D. | HgS+O2$\frac{\underline{\;焙烧\;}}{\;}$ Hg+SO2 |
分析 金属的活动性不同,可以采用不同的冶炼方法.金属冶炼的方法主要有:
热分解法:对于不活泼金属,可以直接用加热分解的方法将金属从其化合物中还原出来,例如2HgO$\frac{\underline{\;\;△\;\;}}{\;}$2Hg+O2↑;
热还原法:在金属活动性顺序表中处于中间位置的金属,通常是用还原剂(C、CO、H2、活泼金属等)将金属从其化合物中还原出来,例如Fe2O3+3CO$\frac{\underline{\;\;△\;\;}}{\;}$2Fe+CO2↑;
电解法:活泼金属较难用还原剂还原,通常采用电解熔融的金属化合物的方法冶炼活泼金属,例如2Al2O3$\frac{\underline{\;电解\;}}{\;}$4Al+3O2↑,以此来解答.
解答 解:A.Mg为活泼金属,利用电解法冶炼,则MgCl2(熔融) $\frac{\underline{\;电解\;}}{\;}$Mg+Cl2↑合理,故A正确;
B.Al为活泼金属,通常用电解熔融的金属化合物的方法冶炼,应为2Al2O3$\frac{\underline{\;电解\;}}{\;}$4Al+3O2↑,故B错误;
C.Fe处于金属活动性顺序表中处于中间位置的金属,通常是用还原剂(C、CO、H2、活泼金属等)将金属从其化合物中还原出来,则Fe2O3+3CO $\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2合理,故C正确;
D.Hg为不活泼金属,可以用HgS与O2焙烧生成Hg,即HgS+O2$\frac{\underline{\;焙烧\;}}{\;}$Hg+SO2合理,故D正确;
故选B.
点评 本题考查金属的冶炼原理,为高考常见题型,侧重于学生的分析能力和应用能力的考查,把握金属活泼性与冶炼原理的关系为解答的关键,题目难度不大.


 初中学业考试导与练系列答案
初中学业考试导与练系列答案科目:高中化学 来源: 题型:解答题
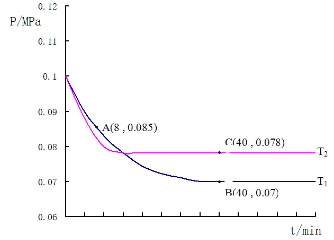 SO2经过净化后与空气混合进行催化氧化后制取硫酸或者硫酸铵,其中SO2发生催化氧化的反应为:2SO2(g)+O2(g)?2SO3(g).若在T1℃、0.1MPa条件下,往一密闭容器通入SO2和O2(其中n(SO2):n(O2)=2:1),测得容器内总压强与反应时间如图所示:
SO2经过净化后与空气混合进行催化氧化后制取硫酸或者硫酸铵,其中SO2发生催化氧化的反应为:2SO2(g)+O2(g)?2SO3(g).若在T1℃、0.1MPa条件下,往一密闭容器通入SO2和O2(其中n(SO2):n(O2)=2:1),测得容器内总压强与反应时间如图所示:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
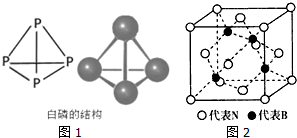 利用周期表中同族元素的相似性,可预测元素的性质.
利用周期表中同族元素的相似性,可预测元素的性质.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
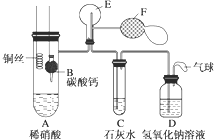
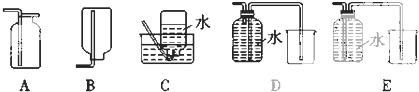
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 18O原子核内的中子数为8 | B. | 16O2和18O2的化学性质几乎相同 | ||
| C. | H216O与H218O质子数不同 | D. | H2和D2属于同位素 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | C3O2分子、COS分子中碳原子可能都采取sp杂化 | |
| B. | C3O2和CO2都是碳的氧化物,它们互为同分异构体 | |
| C. | COS是由极性键构成的非极性分子,分子中所有原子都满足8电子稳定结构 | |
| D. | COS在氧气中完全燃烧,生成物是CO2和SO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ②⑥⑦⑧ | B. | ③④⑤⑥ | C. | ③④⑥⑦ | D. | ①②⑧ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com