
【题目】五氧化二钒(V2O5)在冶金、搪瓷、磁性材料等领域有重要应用。实验室以含钒废料(含V2O3、CuO、MnO、SiO2、A12O3、有机物)为原料制备V2O5的一种流程如图:
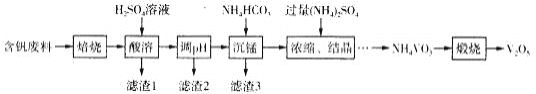
已知I.含钒离子在溶液中的主要存在形式与溶液pH的关系如表所示:

Ⅱ.25℃时,难溶电解质的溶度积常数如表所示:
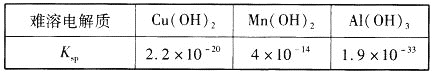
Ⅲ.NH4VO3在水中的溶解度:20℃、4.8g·L-1;60℃、24.2g·L-1。
回答下列问题:
(1)“焙烧”的目的是_____。
(2)“滤渣1”的用途为____(写出一种即可)。
(3)通过计算说明,常温下,若“调pH”为7,Cu2+是否沉淀完全____。(溶液中离子浓度小于10-5mol·L-1时,认为该离子沉淀完全)
(4)“沉锰”需将温度控制在70℃左右,温度不能过高或过低的原因为____。
(5)结晶所得NH4VO3需进行洗涤、干燥。合适的洗涤试剂为____;证明NH4VO3已洗涤干净的实验操作及现象为____。
(6)“煅烧”时生成两种能参与大气循环的气体,该反应的化学方程式为_____。
【答案】除去有机物杂质,将V2O3氧化为V2O5 制光导纤维、制玻璃、制硅胶 “调节pH”为7,溶液中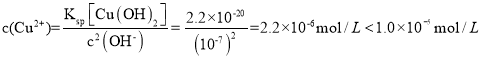 ,Cu2+沉淀完全; 温度过低,反应速率慢,NH4VO3可能提前结晶析出导致产率低;温度过高,NH4HCO3分解导致原料利用率低 冷水 取少量最后一次洗涤液于洁净试管中,滴加BaCl2溶液,无明显现象,证明NH4VO3已洗涤干净 4NH4VO3+3O2
,Cu2+沉淀完全; 温度过低,反应速率慢,NH4VO3可能提前结晶析出导致产率低;温度过高,NH4HCO3分解导致原料利用率低 冷水 取少量最后一次洗涤液于洁净试管中,滴加BaCl2溶液,无明显现象,证明NH4VO3已洗涤干净 4NH4VO3+3O2 ![]() 2V2O5+2N2+8H2O
2V2O5+2N2+8H2O
【解析】
(1)含钒废料中含有有机物杂质,焙烧时会被除去,V2O5是由V2O3制备的,根据V元素化合价的变化分析;
(2)SiO2不与硫酸反应,判断“滤渣1”为SiO2,再写出其用途;
(3)根据溶度积的公式进行计算;
(4)根据温度对反应速率以及对物质的稳定性的影响分析;
(5)根据已知信息NH4VO3的溶解度选择洗涤试剂;检验NH4VO3洗涤干净,只要检验最后一次洗涤液中没有溶液中的硫酸根离子即可;
(6)根据NH4VO3“煅烧”时生成两种能参与大气循环的气体,即产物有V2O5、N2、H2O,据此写出该反应的化学方程式。
(1)焙烧会除去有机物杂质,同时根据V2O3中V元素的化合价为+3价,V2O5中V元素的化合价为+5价知,焙烧还可以将烧V2O3氧化为V2O5;
故答案为:除去有机物杂质,将V2O3氧化为V2O5;
(2)用硫酸酸溶时,SiO2不反应,因此“滤渣1”为SiO2,其用途为制光导纤维、制玻璃、制硅胶等;
故答案为:制光导纤维、制玻璃、制硅胶等(写出一种即可);
(3)调节pH为7,溶液中c(Cu2+)=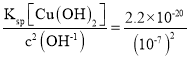 molL-1=2.2×10-6molL-1<10-5molL-1,Cu2+沉淀完全;
molL-1=2.2×10-6molL-1<10-5molL-1,Cu2+沉淀完全;
故答案为:调节pH为7,溶液中c(Cu2+)=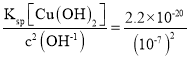 molL-1=2.2×10-6molL-1<10-5molL-1,Cu2+沉淀完全;
molL-1=2.2×10-6molL-1<10-5molL-1,Cu2+沉淀完全;
(4)温度过低,反应速率慢,NH4VO3可能提前结晶析出导致产率低;温度过高,NH4HCO3分解导致原料利用率低;
故答案为:温度过低,反应速率慢,NH4VO3可能提前结晶析出导致产率低;温度过高。NH4HCO3分解导致原料利用率低;
(5)因为NH4VO3在冷水中的溶解度小,在热水中溶解度大,因此选择冷水作洗涤试剂;
若NH4VO3未洗涤干净,则固体上会附着硫酸根离子,因此检验NH4VO3已洗涤干净,只要检验最后一次洗涤液中没有硫酸根离子即可,则实验操作及现象为取少量最后一次洗涤液于洁净试管中,滴加BaCl2溶液,无明显现象,证明NH4VO3已洗涤干净;
故答案为:冷水;取少量最后一次洗涤液于洁净试管中,滴加BaCl2溶液,无明显现象,证明NH4VO3已洗涤干净;
(6)根据“煅烧”时生成两种能参与大气循环的气体,可得该反应的化学方程式为4NH4VO3+3O2![]() 2V2O5+2N2+8H2O;
2V2O5+2N2+8H2O;
故答案为:4NH4VO3+3O2![]() 2V2O5+2N2+8H2O。
2V2O5+2N2+8H2O。


 小学生10分钟口算测试100分系列答案
小学生10分钟口算测试100分系列答案科目:高中化学 来源: 题型:
【题目】下列框图所示的转化关系中,![]() 、
、![]() 均为常见的金属单质;A、
均为常见的金属单质;A、![]() 在冷的
在冷的![]() 的浓溶液中均会发生钝化;
的浓溶液中均会发生钝化;![]() 为淡黄色的非金属单质。
为淡黄色的非金属单质。![]() 为红棕色固体氧化物,
为红棕色固体氧化物,![]() 为常见无色液体。
为常见无色液体。![]() 焰色为黄色,且能使酚酞变红(部分反应条件、反应过程中生成的水及其他产物略去)。
焰色为黄色,且能使酚酞变红(部分反应条件、反应过程中生成的水及其他产物略去)。

(1)![]() 的化学式为______。
的化学式为______。
(2)![]() 与
与![]() 反应的化学方程式为_____。
反应的化学方程式为_____。
(3)![]() 与氯气反应的离子方程式为_____。
与氯气反应的离子方程式为_____。
(4)![]() 与氨水反应的化学方程式为_______。
与氨水反应的化学方程式为_______。
(5)![]() 与
与![]() 反应的离子方程式为________。
反应的离子方程式为________。
(6)检验“黄色溶液”中阳离子的方案:________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.某微粒的结构示意图为![]() ,试回答:
,试回答:
(1)当y=8时,该粒子可能是_____、_____(分别写出一种阳离子和一种阴离子)。
(2)当x-y=10时,该粒子为_______(选填“原子”或“阳离子”、“阴离子”)。
(3)请写出工业上制取y=7元素对应单质的化学方程式:________________。
Ⅱ.现有 ①BaCl2晶体 ②金刚石 ③碘片 ④干冰 ⑤二氧化硅 ⑥氢氧化钾 ⑦钠 七种物质,请按下列要求回答(填序号):
(1)属于只含离子键的离子晶体的是____________(填序号,下同)。
(2)属于分子晶体的单质是__________。
(3)属于原子晶体的化合物是___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物A是合成二氢荆芥内酯的重要原料,其结构简式如下图,下列检验A中官能团的试剂和顺序正确的是( )

A. 先加酸性高锰酸钾溶液,后加银氨溶液,微热
B. 先加溴水,后加酸性高锰酸钾溶液
C. 先加银氨溶液,微热,再加入溴水
D. 先加入新制氢氧化铜,微热,酸化后再加溴水
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图为一种天然产物,具有一定的除草功效。下列有关该化合物的说法错误的是

A. 分子中含有三种含氧官能团
B. 1mol该化合物最多能与4molNaOH反应
C. 既可以发生取代反应,又能够发生加成反应
D. 既能与FeCl3发生显色反应,也能和NaHCO3反应放出CO2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】卤代烃 R—CH2—CH2—X 中化学键如图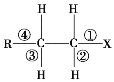 所示,则下列说法正确的是()
所示,则下列说法正确的是()
A. 发生水解反应时,被破坏的键是①和③
B. 发生消去反应时,被破坏的键是①和④
C. 发生水解反应时,被破坏的键是①
D. 发生消去反应时,被破坏的键是①和②
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铟产业被称为“信息时代的朝阳产业”。元素周期表中铟的数据见图,下列说法完全正确的是
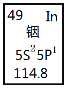
A.铟元素的质量数是114.8
B.铟元素的相对原子质量是115,中子数为66
C.铟元素是一种主族元素,位于第五周期第ⅢA族
D.铟原子最外层有3个能量相同的电子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某有机物是药物生产的中间体,其结构简式如图。下列有关叙述正确的是
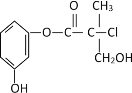
A.该有机物与溴水可发加成反应
B.该有机物与浓硫酸混合共热可发生消去反应
C.1 mol该有机物与足量NaOH溶液反应最多消耗3molNaOH
D.该有机物经催化氧化后与新制氢氧化铜悬浊液共热生成砖红色沉淀
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验装置不能达到实验目的的是
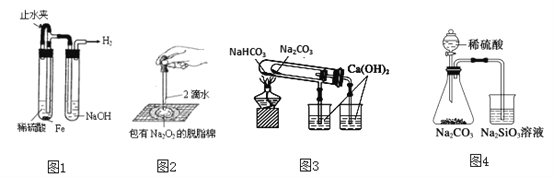
A. 图1:制备并观察氢氧化亚铁
B. 图2:证明过氧化钠与水反应放热
C. 图3:验证NaHCO3和Na2CO3的热稳定性
D. 图4:验证酸性强弱H2SO4>H2CO3>H2SiO3
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com