【答案】
分析:A.原子得失电子变离子,变化的是核外的电子,核内质子数不变;
B.球棍模型主要体现的是分子的空间结构和成键类型,比例模型主要体现的是组成该分子的原子间的大小关系与原子间连接;
C.氢氧化钠是离子化合物,由钠离子与氢氧根负离子构成,氢氧根负离子应加中括号[],在右上角注明电荷;
D.次氯酸中氧原子与氯原子、氢原子之间分别形成1对共用电子对.
解答:解:A.由Cl原子得1个电子变为Cl
-离子,变化的是核外的电子,核内质子数不变,Cl
-离子的结构示意图为
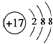
,故A错误;
B.图为CH
4分子的比例模型,故B错误;
C.NaOH的电子式:
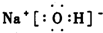
,故C错误;
D.次氯酸中氧原子与氯原子、氢原子之间分别形成1对共用电子对,结构式为H-O-Cl,故D正确.
故选D.
点评:本题考查电子式、原子结构示意图、比例模型、结构式等,难度不大,要明确用电子式表示离子化合物、共价化合物、阴离子及单质分子的方法.

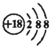

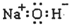
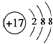 ,故A错误;
,故A错误; 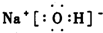 ,故C错误;
,故C错误;
